Wirkstoffe: Beclomethason (Dipropionat), Neomycin (Neomycinsulfat)
MENADERM 0,25 mg/g + 5 mg/g Creme
MENADERM 0,25 mg / g + 5 mg / g Salbe
MENADERM 0,25 mg / g + 5 mg / g Lösung auf der Haut
Warum wird Menaderm verwendet? Wofür ist das?
MENADERM enthält die Wirkstoffe Betachlomethason, die zur Klasse der Kortikosteroide (entzündungshemmende Medikamente) und Neomycin (Antibiotikum) gehören.
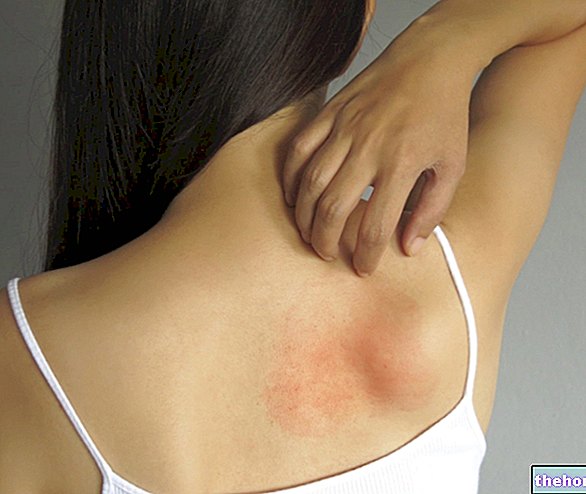
MENADERM wird zur Behandlung von Hauterkrankungen eingesetzt, bei denen eine Therapie mit lokalen Kortikosteroiden angezeigt ist und die durch Infektionen mit Neomycin-empfindlichen Keimen erschwert werden, wie:
- Allergische und entzündliche Dermatitis (allergische oder entzündliche Hautentzündungen), akut und chronisch (kurz oder lang anhaltend), exogen und endogen (verursacht durch äußere oder innere Einwirkungen).
- Kontaktdermatitis verschiedener Art, Ekzeme (juckende Entzündungsreaktion der Haut) bei Kindern und ekzematöse Dermatitis, erythematös-exsudierende Hauterkrankungen (mit Produktion von Exsudat, einer Flüssigkeit, die sich bei Entzündungen bildet).
- Pustulöse Akne (mit begrenzten Hautläsionen, Relief).
- Intertrigo (Hautpathologie, die durch das kontinuierliche Reiben zweier benachbarter Körperoberflächen verursacht wird).
Kontraindikationen Wenn Menaderm nicht angewendet werden sollte
Verwenden Sie MENADERM® nicht
- wenn Sie allergisch gegen die Wirkstoffe oder einen der sonstigen Bestandteile dieses Arzneimittels sind (aufgelistet in Abschnitt 6).
- wenn Sie eine tuberkulöse (durch Tuberkulose bedingte), virale (durch ein Virus verursachte) und luetische (durch Syphilis, eine überwiegend sexuell übertragbare Infektionskrankheit) hervorgerufene Hautläsion haben.
- Als Okklusivverband (Abdecken des betroffenen Bereichs mit Verbänden nach Anwendung des Arzneimittels) bei atopischer Dermatitis (chronisch entzündliche Hauterkrankung mit starkem Juckreiz und Trockenheit) (siehe „Warnhinweise und Vorsichtsmaßnahmen“).
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Menaderm beachten?
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie MENADERM anwenden.
Die Anwendung von Produkten zur topischen Anwendung, insbesondere bei längerer Anwendung, kann zu Sensibilisierungserscheinungen (erhöhte Reaktivität gegenüber einigen Substanzen) führen; in diesem Fall ist es erforderlich, dass Sie die Behandlung abbrechen und Ihr Arzt wird eventuell eine adäquate Therapie des Bewusstseinsphänomens einleiten das ist passiert.
Bei der okklusiven Therapie, insbesondere bei ausgedehnten Läsionen, ist es ratsam, jeweils nur eine Teilbehandlung durchzuführen, da diese Technik die Aufnahme der Komponenten begünstigen kann mit dem möglichen Auftreten von systemischen Effekten (bezogen auf den gesamten Organismus) ). Durch die Behandlung jeweils eines Bereichs ist es möglich, jegliche Veränderungen der thermischen Homöostase zu vermeiden, die bei einer Erhöhung der Körpertemperatur auftreten können. Wenn solche Veränderungen auftreten, beenden Sie die Behandlung sofort.
Durch das verwendete Material des Okklusivverbandes kann es zu individuellen Sensibilisierungserscheinungen kommen, die einen Ersatz des verwendeten Materials erforderlich machen.
Bei Säuglingen kann die Windel als Okklusivverband fungieren und so das Risiko von Nebenwirkungen erhöhen.
Die okklusive Therapie ist bei atopischer Dermatitis kontraindiziert (siehe „MENADERM darf nicht angewendet werden“). Das Produkt ist nicht für den ophthalmologischen (Augen-) Gebrauch bestimmt.
Kinder und Jugendliche
In den ersten Lebensmonaten sollte die Anwendung von MENADERM nur bei wirklicher Notwendigkeit und unter direkter Aufsicht des Arztes erfolgen.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Menaderm® verändern?
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel anwenden, kürzlich andere Arzneimittel angewendet haben oder beabsichtigen andere Arzneimittel einzunehmen.
Es sind keine Arzneimittelwechselwirkungen mit MENADERM bekannt.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Wenn Sie schwanger sind oder stillen, verwenden Sie MENADERM nur im wirklichen Bedarfsfall und unter direkter ärztlicher Aufsicht, insbesondere bei großflächiger Anwendung oder mit Okklusivverband.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Es sind keine Auswirkungen auf die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen nach der Anwendung von MENADERM bekannt.
MENADERM enthält Ester der p-Hydroxybenzoesäure, die (auch verzögert) allergische Reaktionen hervorrufen können.
Dosis, Methode und Zeitpunkt der Verabreichung Wie ist Menaderm anzuwenden: Dosierung
Wenden Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker an. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Tragen Sie zweimal täglich eine kleine Menge des Produkts (dünne Schicht) auf die betroffene Hautpartie auf und massieren Sie es sanft ein.
Der Okklusivverband kann im Einzelfall nach Ermessen des Arztes angebracht sein.
MENADERM Creme wird bevorzugt bei der Behandlung von empfindlichen oder feuchten Hautoberflächen verwendet.
MENADERM Salbe ist indiziert bei der Behandlung von trockenen, lichenifizierten (verdickten) oder schuppigen Läsionen und bei Verwendung von Okklusivverbänden.
MENADERM Lösung zur Anwendung auf der Haut ist indiziert zur Behandlung ausgedehnter Hautläsionen, Hautfalten und behaarter Bereiche (mit Haaren).
Überdosierung Was ist zu tun, wenn Sie zu viel Menaderm eingenommen haben?
Es sind keine Fälle von Überdosierung nach der Anwendung von MENADERM bekannt.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Nebenwirkungen Was sind die Nebenwirkungen von Menaderm®
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Brechen Sie die Behandlung ab und wenden Sie sich an Ihren Arzt, der Ihnen eine geeignete Therapie verschreiben wird, wenn Sie eine der unten aufgeführten Nebenwirkungen bemerken:
- Brennen, Reizung, Trockenheit der Haut, Follikulitis (Hautinfektionen), akneiforme Ausschläge (akneähnliche Hautausschläge), Hypertrichose (vermehrte Behaarung), Hypopigmentierung (Verfärbung der Haut) und insbesondere bei okklusiven Verbänden Hautatrophie ( Ausdünnung der Haut). Diese Effekte sind klassische Störungen im Zusammenhang mit einer lokalen Kortikosteroidtherapie (Kortikosteroidtherapie) und treten meist in leichter und reversibler Form auf. Sie können durch eine okklusive Therapie oder durch dosierte Anwendung des Arzneimittels und über einen längeren Zeitraum begünstigt werden auf großen Hautpartien (siehe „Warnhinweise und Vorsichtsmaßnahmen“).
- Entwicklung von unempfindlichen Mikroorganismen (die nicht auf die Behandlung mit MENADERM ansprechen), einschließlich Pilzen (Pilze), die bei längerer Anwendung des Antibiotikums (Neomycin) auftreten können.
Das Auftreten systemischer Nebenwirkungen durch Kortikosteroide ist sehr unwahrscheinlich.
Wenn jedoch Ihre Nierenfunktion beeinträchtigt ist, kann es in Ausnahmefällen zu Ototoxizitätsphänomenen (Toxizität auf Höhe der Ohren) und Nephrotoxizität (Nierentoxizität) aufgrund einer systemischen Reabsorption (Übergang ins Blut) von Neomycin kommen.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über die italienische Arzneimittelbehörde melden, Website: http://www.agenziafarmaco.gov.it/it/responsabili Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Verwenden Sie dieses Arzneimittel nicht nach dem auf der Packung angegebenen Verfallsdatum. Das Verfallsdatum bezieht sich auf den letzten Tag des Monats und auf das Produkt in intakter Verpackung, sachgemäß gelagert MENADERM Creme und MENADERM Salbe.
Unter 30 °C lagern.
MENADERM-kutane Lösung.
Es sind keine besonderen Aufbewahrungsvorkehrungen erforderlich.
Werfen Sie Arzneimittel nicht in das Abwasser oder den Hausmüll. Fragen Sie Ihren Apotheker, wie Sie Arzneimittel, die Sie nicht mehr verwenden, entsorgen. Dies trägt zum Schutz der Umwelt bei.
Frist "> Weitere Informationen
Was MENADERM enthält
MENADERM-Creme
1 g Sahne enthält:
Wirkstoffe: Beclomethasondipropionat 0,25 mg, Neomycinsulfat 5 mg.
Andere Bestandteile: Glycerylmonostearat, Cetomacrogol, flüssiges Paraffin, weiße Vaseline, Isopropylmyristat, Myristylalkohol, Ester der p-Hydroxybenzoesäure, gereinigtes Wasser.
MENADERM-Salbe
1 g Salbe enthält:
Wirkstoffe: Beclomethasondipropionat 0,25 mg, Neomycinsulfat 5 mg.
Andere Bestandteile: Decyloleat, flüssiges Paraffin, Ester der p-Hydroxybenzoesäure, weiße Vaseline.
MENADERM Lösung für die Haut
1 g Hautlösung enthält:
Wirkstoffe: Beclomethasondipropionat 0,25 mg, Neomycinsulfat 5 mg.
Andere Bestandteile: Glycerylmonostearat, Cetomacrogol, flüssiges Paraffin, weiße Vaseline, Isopropylmyristat, Myristylalkohol, Ester der p-Hydroxybenzoesäure, gereinigtes Wasser.
Beschreibung wie MENADERM aussieht und Inhalt der Packung
MENADERM-Creme
Creme. 30 g Tube mit einer Creme von weicher, weißer, homogener Konsistenz, praktisch geruchlos.
MENADERM-Salbe
Salbe. 30 g Tube mit einer Salbe von weicher Konsistenz, weiß-grau, homogen, fettig, praktisch geruchlos.
MENADERM Lösung für die Haut
Hautlösung. 30 g Flasche mit Tropfer, die eine halbflüssige, weiße, homogene, praktisch geruchlose Lotion enthält.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS -
MENADERM CREME - HAUTLÖSUNG.
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG -
MENADERM CREME
1 g enthält:
Beclomethasondipropionat 0,25 mg, Neomycinsulfat 5 mg.
Sonstige Bestandteile mit bekannter Wirkung: p-Hydroxybenzoesäureester
MENADERM HAUTLÖSUNG
1 g enthält:
Beclomethasondipropionat 0,25 mg, Neomycinsulfat 5 mg.
Sonstige Bestandteile mit bekannter Wirkung: p-Hydroxybenzoesäureester
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM -
Hautcreme und Lösung.
04.0 KLINISCHE INFORMATIONEN -
04.1 Anwendungsgebiete -
Menaderm ist indiziert zur Behandlung von Hautkrankheiten, bei denen eine lokale Kortikotherapie angezeigt ist und die durch Infektionen mit Neomycin-empfindlichen Keimen kompliziert sind: allergische und entzündliche Dermatitis, akute und chronische, exogene und endogene; Kontaktdermatitis verschiedener Art, infantiles Ekzem und ekzematöse Dermatitis, erythematös exsudierende Hauterkrankungen. Pustulöse Akne, Intertrigo.
04.2 Dosierung und Art der Anwendung -
Im Allgemeinen reichen zwei tägliche Anwendungen von Menaderm auf die betroffene Hautpartie aus, wobei jedes Mal eine kleine Menge des Produkts verwendet und sanft einmassiert wird.
Der Okklusivverband kann im Einzelfall nach ärztlicher Beurteilung angebracht sein.
Die Menaderm-Creme ist aufgrund ihres wassermischbaren Trägers bei der Behandlung empfindlicher oder feuchter Hautoberflächen zu bevorzugen.
Die Menaderm-Hautlösung ist zur Behandlung ausgedehnter Hautläsionen, Hautfalten und Haarpartien indiziert.
04.3 Kontraindikationen -
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile. Die Anwendung von Menaderm ist kontraindiziert bei tuberkulösen, viralen und luetischen Hautläsionen Die Anwendung in der Okklusivtherapie ist bei atopischer Dermatitis kontraindiziert.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung -
Die Anwendung von Produkten zur topischen Anwendung, insbesondere bei längerer Anwendung, kann zu Sensibilisierungserscheinungen führen.In diesem Fall ist eine Unterbrechung der Behandlung und ggf. Einleitung einer geeigneten Therapie unter direkter ärztlicher Aufsicht erforderlich. Das Produkt ist nicht für die Augenheilkunde bestimmt.
Wird die okklusive Verbandstechnik gewählt, ist es ratsam, bei ausgedehnten Läsionen, da sie die Aufnahme der Komponenten begünstigen kann mit der Folge möglicher systemischer Wirkungen auch vermieden werden, die bei einem Anstieg der Körpertemperatur auftreten, der, wenn er auftritt, eine Unterbrechung der Behandlung erfordert. Durch das verwendete Material des Okklusivverbandes kann es zu individuellen Sensibilisierungserscheinungen kommen, die einen Ersatz des verwendeten Materials erforderlich machen. Die okklusive Therapie ist bei atopischer Dermatitis kontraindiziert. Bitte beachten Sie, dass Windeln bei Neugeborenen als Okklusivverband wirken können und somit das Risiko von Nebenwirkungen erhöht.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen -
Nicht bekannt
04.6 Schwangerschaft und Stillzeit -
Bei schwangeren und stillenden Frauen sollte die Anwendung von Menaderm in dringenden Fällen und unter direkter Aufsicht des Arztes erfolgen, insbesondere wenn es großflächig oder mit einem Okklusivverband aufgetragen wird.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen -
Es sind keine Auswirkungen auf die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen nach der Anwendung von MENADERM bekannt.
04.8 Nebenwirkungen -
Systemische Nebenwirkungen von Kortikosteroiden sind unwahrscheinlich. Ihr Erscheinungsbild kann jedoch durch eine okklusive Therapie und wenn große Hautareale mit hohen Dosen und über einen längeren Zeitraum behandelt werden, begünstigt werden. In diesen Fällen handelt es sich um die klassischen Störungen der Kortikotherapie, meist in leichter und reversibler Form.Bei Patienten mit eingeschränkter Nierenfunktion sind Ototoxizitäts- und Nephrotoxizitätsphänomene aufgrund einer systemischen Reabsorption von Neomycin bei Anwendung hoher Dosen auf großen Flächen und über einen längeren Zeitraum, insbesondere unter Okklusivverband, ausnahmsweise möglich. Die lokale Kortikotherapie kann manchmal zu Brennen, Reizungen, trockener Haut, Follikulitis, akneiformen Ausschlägen, Hypertrichose, Hypopigmentierung und insbesondere bei Verwendung des Okklusivverbandes zu Hautatrophie führen. Das mögliche Auftreten der oben genannten Reaktionen erfordert die Unterbrechung der Behandlung und gegebenenfalls die Einleitung einer geeigneten Therapie. Gleiches gilt für die Entwicklung unempfindlicher Mikroorganismen, einschließlich Pilzen, die bei längerer Anwendung des Antibiotikums auftreten können.
Meldung von vermuteten Nebenwirkungen
Die Meldung von vermuteten Nebenwirkungen, die nach der Zulassung des Arzneimittels auftreten, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden. "Adresse www. agenziafarmaco.gov.it/it/responsabili.
04.9 Überdosierung -
Es sind keine Fälle von Überdosierung bekannt.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN -
05.1 "Pharmakodynamische Eigenschaften -
Menaderm ist ein dermatologisches Präparat in zwei Darreichungsformen (Creme und Lösung) zur Behandlung zahlreicher entzündlicher und allergischer Hauterkrankungen, die durch bakterielle Infektionen kompliziert sind. Wirkstoffe des Produkts sind Beclomethason-17,21-dipropionat und Neomycin. Beclometason-17,21-dipropionat ist ein halogeniertes synthetisches Glukokortikoid, das insbesondere topisch mit einer intensiven Antireaktion und antiallergischen Wirkung ausgestattet ist. Im Vasokonstriktionstest der Haut nach McKenzie ist Beclomethason-17,21-dipropionat 5000-mal wirksamer als Hydrocortison Neomycinsulfat ist ein Aminoglykosid-Antibiotikum mit einem breiten antibakteriellen Wirkungsspektrum.
05.2 "Pharmakokinetische Eigenschaften -
Absorption
Sowohl Beclomethason-17,21-dipropionat als auch Neomycin werden nach Anwendung auf der Haut in der Regel nicht in nennenswerten Mengen resorbiert und entfalten ihre Wirkung nur lokal.
Bei Behandlungen großer Hautareale mit hohen Dosen und insbesondere bei Verwendung eines Okklusivverbandes kann es jedoch vorkommen, dass die perkutane Resorption einen nicht mehr zu vernachlässigenden Charakter annimmt.
Biotransformation
Der schließlich resorbierte Teil des Steroids wird in der Leber in inaktive Metaboliten umgewandelt, was die hohe Verträglichkeit von Beclomethason-17,21-dipropionat weiter begründet.
05.3 Präklinische Daten zur Sicherheit -
Menaderm, das 28 Tage lang auf die Haut von Ratten in einer Dosis von 3 g / kg / Tag aufgetragen wurde, wurde sowohl lokal als auch systemisch gut vertragen (insbesondere keine Unterdrückung der Nebennierenrindenaktivität).
06.0 PHARMAZEUTISCHE INFORMATIONEN -
06.1 Hilfsstoffe -
MENADERM CREME
Glycerylmonostearat, Cetomacrogol, flüssiges Paraffin, weiße Vaseline, Isopropylmyristat, Myristylalkohol, Ester der p-Hydroxybenzoesäure, gereinigtes Wasser.
MENADERM HAUTLÖSUNG
Glycerylmonostearat, Cetomacrogol, flüssiges Paraffin, weiße Vaseline, Isopropylmyristat, Myristylalkohol, Ester der p-Hydroxybenzoesäure, gereinigtes Wasser.
06.2 Inkompatibilität "-
Spezifische Unverträglichkeiten sind nicht bekannt.
06.3 Gültigkeitsdauer "-
48 Monate.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung -
Unter 30 °C lagern.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks -
MENADERM CREME
30g weiche Aluminiumtube.
MENADERM HAUTLÖSUNG
30-g-Flasche und Polyäthylen-Tropfflasche und Polypropylen-Schraubverschluss.
06.6 Gebrauchs- und Handhabungshinweise -
Keine besonderen Anweisungen
07.0 INHABER DER "MARKETING GENEHMIGUNG" -
A. Menarini Industrie Farmaceutiche Riunite s.r.l. - Via Sette Santi 3, Florenz.
08.0 NUMMER DER VERMARKTUNGSBERECHTIGUNG -
MENADERM CREME - A.I.C. n. 020883094.
MENADERM HAUTLÖSUNG - A.I.C. n. 020883118.
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG -
Datum der Erstzulassung: 21. April 1986
Datum der letzten Verlängerung: 31. Mai 2010
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs -
September 2016