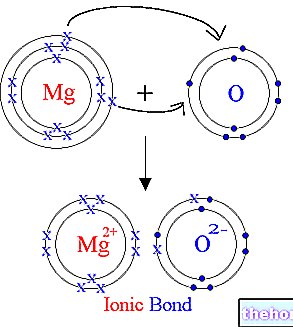
Wirkstoffe: Dienogest, Ethinylestradiol
Effiprev 2 mg / 0,03 mg Filmtabletten
Warum wird Effiprev verwendet? Wofür ist das?
Wichtige Informationen zu kombinierten hormonalen Kontrazeptiva (KOK):
- Sie sind bei richtiger Anwendung eine der zuverlässigsten reversiblen Verhütungsmethoden
- Sie erhöhen leicht das Risiko von Blutgerinnseln in den Venen und Arterien, insbesondere im ersten Jahr der Einnahme oder bei Wiederaufnahme eines kombinierten hormonalen Kontrazeptivums nach einer Pause von 4 oder mehr Wochen
- Seien Sie vorsichtig und suchen Sie Ihren Arzt auf, wenn Sie glauben, Symptome eines Blutgerinnsels zu haben (siehe Abschnitt 2 „Blutgerinnsel“).
Was ist Effiprev und wofür ist es?
Effiprev Filmtabletten (kurz Effiprev genannt) sind ein orales Kontrazeptivum, das eine „Kombination von zwei Hormonen“ enthält.
Effiprev enthält in geringen Mengen zwei Arten weiblicher Sexualhormone, nämlich Ethinylestradiol (mit ähnlichen Wirkungen wie Östrogen) und Dienogest (das ähnliche Wirkungen wie das natürliche Lutealhormon Progesteron hat). Medikament gehört zur Familie der "Mikropillen", kombinierte hormonale Kontrazeptiva, bestehend aus zwei Arten von Hormonen, monophasisch, dh in allen Tabletten die gleichen Mengen enthalten
Kontraindikationen Wenn Effiprev nicht angewendet werden sollte
Orale Kontrazeptiva und Krebsrisiko
Brustkrebs wurde bei Frauen, die die Pille einnehmen, etwas häufiger festgestellt als bei Frauen, die dies nicht tun, obwohl nicht sicher ist, ob dies auf die Einnahme der Pille zurückzuführen ist in einem früheren Stadium als bei anderen Frauen mit der gleichen Krebserkrankung.
10 Jahre nach Absetzen der Pille verschwindet dieser kleine Unterschied.
In seltenen Fällen wurde bei Frauen, die die Pille einnehmen, über gutartige Lebertumoren – und noch seltener über bösartige Lebertumoren – berichtet. Diese Tumoren können innere (Bauch-)Blutungen verursachen. Wenn Sie starke Schmerzen im Oberbauch verspüren, sollten Sie sofort Ihren Arzt aufsuchen.
Einige Studien haben gezeigt, dass Frauen, die die Pille über einen längeren Zeitraum einnehmen, häufiger an Gebärmutterhalskrebs erkranken. Es ist jedoch nicht ganz sicher, dass dies durch die Pille verursacht wird, da die Inzidenz von Gebärmutterhalskrebs von vielen anderen Faktoren beeinflusst wird, wie beispielsweise dem Sexualverhalten (zB häufiger Partnerwechsel).
Verwenden Sie Effiprev nicht:
Verwenden Sie Effiprev nicht, wenn Sie eine der unten aufgeführten Erkrankungen haben. Wenn Sie eine der unten aufgeführten Erkrankungen haben, wenden Sie sich bitte an Ihren Arzt. Ihr Arzt wird mit Ihnen andere Verhütungsmethoden besprechen, die für Sie möglicherweise besser geeignet sind.
- wenn Sie ein Blutgerinnsel in einem Blutgefäß des Beines (tiefe Venenthrombose, TVT), der Lunge (Lungenembolie, LE) oder eines anderen Organs haben (oder hatten);
- wenn Sie wissen, dass Sie an einer Erkrankung leiden, die die Blutgerinnung beeinflusst, wie Protein-C-Mangel, Protein-S-Mangel, Antithrombin-III-Mangel, Faktor-V-Leiden oder Antiphospholipid-Antikörper;
- wenn bei Ihnen eine "Operation" ansteht oder Sie längere Zeit liegen bleiben (siehe Abschnitt "Blutgerinnsel");
- wenn Sie jemals einen Herzinfarkt oder Schlaganfall hatten;
- wenn Sie Angina pectoris (eine Erkrankung, die starke Brustschmerzen verursacht und ein erstes Anzeichen für einen Herzinfarkt sein kann) oder eine vorübergehende ischämische Attacke (TIA – vorübergehende Schlaganfallsymptome) haben (oder jemals hatten);
- wenn Sie an einer der folgenden Erkrankungen leiden, die das Risiko von Blutgerinnseln in den Arterien erhöhen können:
- schwerer Diabetes mit Gefäßverletzung
- sehr hoher Blutdruck oder sehr hohe Blutfettwerte (Cholesterin oder Triglyceride)
- eine Krankheit, die als Hyperhomocysteinämie bekannt ist
- wenn Sie eine Art von Migräne namens „Migräne mit Aura“ haben (oder jemals hatten);
- wenn Sie allergisch gegen Ethinylestradiol, Dienogest oder einen der in Abschnitt 6. genannten sonstigen Bestandteile dieses Arzneimittels sind;
- schwere aktive Lebererkrankung, Gelbsucht im Gange oder in Ihrer Familienanamnese vorhanden; Gelbsucht oder Juckreiz im ganzen Körper können die ersten Anzeichen einer Lebererkrankung sein;
- Lebertumor in aktiver Phase (gutartig oder bösartig) oder in seiner Familienanamnese vorhanden;
- bekannte oder vermutete Krebserkrankungen der Geschlechtsorgane oder der Brust;
- vaginale Blutungen unbekannter Herkunft;
- Pankreatitis oder Pankreatitis in der Vorgeschichte, wenn sie mit schwerer Hypertriglyzeridämie einhergeht;
- schweres Nierenversagen oder akutes Nierenversagen;
Wenn Sie an einer der oben aufgeführten Erkrankungen leiden, informieren Sie Ihren Arzt, bevor Sie mit der Einnahme von Effiprev beginnen. Ihr Arzt wird Ihnen möglicherweise eine andere Art der oralen Verhütungspille oder eine andere nicht-hormonelle Verhütungsmethode vorschlagen.
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Effiprev® beachten?
Bevor Sie mit der Anwendung von Effiprev beginnen, sollten Sie die Informationen zu Blutgerinnseln lesen. Es ist besonders wichtig, die Symptome eines Blutgerinnsels zu lesen (siehe Abschnitt „Blutgerinnsel“).
In dieser Packungsbeilage sind verschiedene Szenarien aufgeführt, wann die Einnahme von Effiprev beendet oder in welchen Situationen die empfängnisverhütende Wirkung verringert werden kann. In diesen Fällen müssen Sie auf Geschlechtsverkehr verzichten oder nicht-hormonelle Verhütungsmittel (z. Verwenden Sie keine Methoden, die auf biologischen Rhythmen oder der Erfassung der Körpertemperatur basieren, da diese Methoden unzuverlässig sein können.
Wie bei anderen kombinierten oralen Kontrazeptiva schützt die Einnahme von Effiprev nicht vor einer HIV-Infektion (AIDS) oder anderen sexuell übertragbaren Krankheiten.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Effiprev® beeinflussen
Einnahme von Effiprevi zusammen mit anderen Arzneimitteln
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel einnehmen, kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen andere Arzneimittel einzunehmen.
Einige Arzneimittel können die Wirksamkeit von KOK beeinträchtigen.Eines der ersten Anzeichen dafür können abnormale Genitalblutungen sein.Zu diesen Arzneimitteln gehören:
- Carbamazepin, Oxycarbamazepin, Topiramat und Felbamat);
- Arzneimittel zur Behandlung von Tuberkulose (z. B. Rifampicin);
- Antibiotika zur Behandlung einiger Infektionen (z. B. Ampicillin, Tetracyclin, Griseofulvin);
- Ritonavir, Rifabutin, Efavirenz, Nevirapin, Nelvinafir);
- das pflanzliche Präparat namens Johanniskraut (Hypericum perforatum).
Bestimmte Medikamente und Grapefruitsaft können die Plasmaspiegel von Dienogest beeinflussen (z. B. Azol-Antimykotika, Cimetidin, Verapamil, Diltiazem, Makrolide, Antidepressiva).
KOK können auch die Wirksamkeit einiger Arzneimittel beeinträchtigen, zB Arzneimittel, die Ciclosporin oder Lamotrigin enthalten.Die Gestagenverbindung kann die Wirkung einiger blutdrucksenkender Arzneimittel (blutdrucksenkender Arzneimittel) und nichtsteroidaler entzündungshemmender Arzneimittel beeinträchtigen.
Informieren Sie den Arzt, der andere Arzneimittel verschreibt, und auch den Zahnarzt, dass Sie Effiprev einnehmen. Ihr Arzt wird Ihnen sagen, ob Sie andere nicht-hormonelle Verhütungsmethoden anwenden müssen und wie lange Sie diese anwenden müssen.
Frauen, die eine Kurzzeitbehandlung (maximale Dauer von einer Woche) mit den oben genannten Arzneimitteln erhalten, müssen zusätzliche empfängnisverhütende Maßnahmen ergreifen, z. Barrieremethode (Kondom) während der gleichzeitigen Anwendung des Begleitmedikaments und in den 7 Tagen nach dem Absetzen.
Die gleichzeitige Behandlung mit Rifampicin erfordert die Anwendung zusätzlicher empfängnisverhütender Maßnahmen (z. B. eine Barrieremethode) während der Einnahme des gleichzeitigen Arzneimittels und für 28 Tage nach dessen Absetzen. Wenn die gleichzeitige Anwendung des Arzneimittels auch nach Beendigung einer kombinierten hormonalen Kontrazeptiva-Packung fortgesetzt wird, sollte die nächste Packung des kombinierten hormonalen Kontrazeptivums ohne Einhaltung des üblichen tablettenfreien Intervalls begonnen werden.
Informieren Sie Ihren Arzt, wenn Sie über längere Zeit Arzneimittel zur Induktion des Leberenzymsystems einnehmen (lesen Sie auch die Packungsbeilagen der anderen Produkte). In einigen Fällen kann es notwendig sein, eine nicht-hormonelle Verhütungsmethode zu wählen.
Warnungen Es ist wichtig zu wissen, dass:
Wann sollten Sie einen Arzt aufsuchen?
Dringend einen Arzt aufsuchen
- wenn Sie mögliche Anzeichen eines Blutgerinnsels bemerken, die darauf hinweisen können, dass Sie an einem Blutgerinnsel im Bein (tiefe Venenthrombose), einem Blutgerinnsel in der Lunge (Lungenembolie), einem Herzinfarkt oder einem Schlaganfall leiden (siehe Abschnitt unten). „Blutgerinnsel“).
Eine Beschreibung der Symptome dieser schwerwiegenden Nebenwirkungen finden Sie im Abschnitt „Wie man ein Blutgerinnsel erkennt“.
Informieren Sie Ihren Arzt, wenn einer der folgenden Punkte auf Sie zutrifft. Wenn dieser Zustand während der Anwendung von Effiprev auftritt oder sich verschlimmert, sollten Sie Ihren Arzt informieren.
- wenn Sie an Morbus Crohn oder Colitis ulcerosa (chronisch entzündliche Darmerkrankung) leiden;
- wenn Sie systemischen Lupus erythematodes (SLE, eine Krankheit, die das natürliche Abwehrsystem beeinträchtigt) haben;
- wenn Sie ein hämolytisch-urämisches Syndrom (HUS, eine Blutgerinnungsstörung, die zu Nierenversagen führt) haben;
- wenn Sie an Sichelzellenanämie (eine Erbkrankheit der roten Blutkörperchen) leiden;
- wenn Sie hohe Blutfettwerte (Hypertriglyzeridämie) haben oder eine „positive Familienanamnese dieser Erkrankung“ aufweisen.
- wenn Sie sich einer „Operation unterziehen“ oder wenn Sie sich für längere Zeit hinlegen (siehe Abschnitt 2 „Blutgerinnsel“);
- Wenn Sie gerade erst entbunden haben, ist Ihr Risiko für die Bildung von Blutgerinnseln höher. Fragen Sie Ihren Arzt, wann Sie nach der Geburt mit der Einnahme von Effiprev beginnen können.
- wenn Sie eine "Entzündung der Venen unter der Haut (oberflächliche Thrombophlebitis)" haben;
- wenn Sie Krampfadern haben.
- wenn Sie Diabetes mellitus haben;
- wenn Sie an Fettleibigkeit leiden (Body-Mass-Index über 30 kg / m2);
- wenn er seine endgültige Erwachsenengröße noch nicht erreicht hat;
- wenn Sie an Bluthochdruck leiden;
- wenn Sie an einer Herzklappenerkrankung oder Herzrhythmusstörungen leiden;
- wenn einer Ihrer nahen Verwandten eine Thrombose, einen Herzinfarkt oder einen Schlaganfall hatte;
- wenn Sie an Migräne leiden;
- wenn Sie an Krampfanfällen (Epilepsie, Sydenham-Chorea) leiden;
- wenn Sie an einer Leber- oder Gallenerkrankung leiden;
- wenn Sie an Gelbsucht und/oder Juckreiz am ganzen Körper leiden;
- wenn Sie an einer seltenen Störung des Hämoglobinstoffwechsels (Porphyrie) leiden;
- wenn Sie an einem hereditären Angioödem leiden;
- wenn Sie an einer endogenen Depression leiden;
- wenn Sie im späten Stadium der Schwangerschaft (Gestationsherpes) jemals einen „Blasenausschlag“ hatten;
- wenn Sie an Hörproblemen leiden, die als Otosklerose bekannt sind;
- wenn Sie bräunlich-gelbe Flecken auf der Haut, insbesondere im Gesicht (Chloasma) haben oder hatten; Wenn Sie von diesem Problem betroffen sind, müssen Sie es vermeiden, sich direktem Sonnenlicht oder ultraviolettem Licht auszusetzen.
- wenn du rauchst. Das Rauchen von Zigaretten erhöht das Risiko schwerwiegender Nebenwirkungen im Zusammenhang mit der Anwendung oraler Kontrazeptiva wie Herzinfarkt und Schlaganfall.Das Risiko erhöht sich weiter, wenn Sie starker Raucher sind und mit zunehmendem Alter.
Wenn Sie die Pille einnehmen, hören Sie auf zu rauchen, insbesondere wenn Sie über 35 Jahre alt sind. Wenn Sie nicht beabsichtigen, mit dem Rauchen aufzuhören, sollten Sie andere Verhütungsmethoden anwenden, insbesondere wenn noch andere Risikofaktoren vorliegen.
Wann es angebracht ist, medizinische Untersuchungen durchzuführen
Ihr Arzt wird Ihnen möglicherweise empfehlen, während der Einnahme der Pille regelmäßige medizinische Untersuchungen durchzuführen. Abhängig von Ihrem Gesundheitszustand und Ihrem Gesundheitszustand entscheidet der Arzt über die Häufigkeit dieser Kontrollen und die Art der durchzuführenden Tests.
Wenden Sie sich so schnell wie möglich an Ihren Arzt, wenn einer der folgenden Punkte auftritt:
- wenn Sie eine Veränderung Ihres Gesundheitszustandes bemerken (überprüfen Sie insbesondere die in dieser Packungsbeilage beschriebenen Symptome) oder wenn die in der Packungsbeilage genannten Erkrankungen bei einem Familienmitglied auftreten;
- wenn Sie beim Abtasten der Brust einen Knoten bemerken;
- wenn Sie andere Arzneimittel einnehmen müssen;
- vor einer geplanten Operation oder im Falle einer Ruhigstellung (wenden Sie sich mindestens 4 Wochen vorher an Ihren Arzt);
- wenn bei Ihnen ungewöhnlich starke und unregelmäßige Blutungen aus der Scheide auftreten;
- wenn Sie in der ersten Behandlungswoche die Einnahme einer oder mehrerer Tabletten vergessen haben oder in den letzten 7 Tagen Geschlechtsverkehr hatten;
- wenn zweimal hintereinander keine Abbruchblutung aufgetreten ist oder wenn Sie vermuten, schwanger zu sein (die KOK-Anwendung kann wieder aufgenommen werden, wenn Ihr Arzt dies für angemessen hält).
BLUTGERINNSEL
Die Anwendung eines kombinierten hormonalen Kontrazeptivums wie Effiprev erhöht Ihr Risiko für die Bildung eines Blutgerinnsels im Vergleich zur Nichtanwendung eines Blutgerinnsels.In seltenen Fällen kann ein Blutgerinnsel Blutgefäße verstopfen und schwerwiegende Probleme verursachen.
Blutgerinnsel können entstehen
- in Venen (sogenannte „Venenthrombose“, „venöse Thromboembolie“ oder VTE)
- in den Arterien (als „arterielle Thrombose“, „arterielle Thromboembolie“ oder ATE bezeichnet).
Die Erholung von Blutgerinnseln ist nicht immer vollständig. In seltenen Fällen können lang anhaltende schwere Wirkungen auftreten oder sehr selten tödlich sein.
Es ist wichtig, sich daran zu erinnern, dass das Gesamtrisiko eines schädlichen Blutgerinnsels im Zusammenhang mit der Anwendung von Effiprev gering ist
WIE MAN EIN BLUTGERINNSEL ERKENNT
Suchen Sie sofort einen Arzt auf, wenn Sie eines der folgenden Anzeichen oder Symptome bemerken.
- Schwellung eines Beines oder entlang einer Bein- oder Fußvene, insbesondere in Verbindung mit:
- Schmerzen oder Druckempfindlichkeit im Bein, die nur beim Stehen oder Gehen zu spüren sind
- verstärktes Hitzegefühl im betroffenen Bein
- Veränderung der Hautfarbe am Bein, wie zum Beispiel blass, rot oder blau
- plötzliche und unerklärliche Kurzatmigkeit oder schnelle Atmung;
- plötzlicher Husten ohne offensichtliche Ursache, möglicherweise Blutaustritt;
- stechender Brustschmerz, der mit tiefer Atmung zunehmen kann;
- schwere Benommenheit oder Schwindel;
- schneller oder unregelmäßiger Herzschlag;
- starke Schmerzen im Magen
- sofortiger Verlust des Sehvermögens
- schmerzloses verschwommenes Sehen, das zum Verlust des Sehvermögens führen kann
- Brustschmerzen, Unwohlsein, Druck- oder Schweregefühl
- Quetsch- oder Völlegefühl in Brust, Arm oder unterhalb des Brustbeins;
- Völlegefühl, Verdauungsstörungen oder Erstickungsgefühl;
- Oberkörperbeschwerden mit Ausstrahlung in Rücken, Kiefer, Rachen, Arme und Bauch;
- Schwitzen, Übelkeit, Erbrechen oder Schwindel;
- extreme Schwäche, Angst oder Kurzatmigkeit;
- schneller oder unregelmäßiger Herzschlag
- plötzliche Taubheit oder Schwäche des Gesichts, Arms oder Beins, insbesondere auf einer Körperseite;
- plötzliche Verwirrung, Schwierigkeiten beim Sprechen oder Verstehen;
- plötzliche Schwierigkeiten beim Sehen auf einem oder beiden Augen;
- plötzliche Schwierigkeiten beim Gehen, Schwindel, Gleichgewichts- oder Koordinationsverlust;
- plötzliche, schwere oder anhaltende Migräne ohne bekannte Ursache;
- Bewusstlosigkeit oder Ohnmacht mit oder ohne Krampfanfälle.
- Schwellung und blassblaue Verfärbung einer Extremität;
- starke Bauchschmerzen (akuter Bauch)
BLUTGERINNSEL IN EINER VENE
Was kann passieren, wenn sich ein Blutgerinnsel in einer Vene bildet?
- Die Anwendung kombinierter hormonaler Kontrazeptiva wurde mit einem erhöhten Risiko für die Bildung von Blutgerinnseln in den Venen (Venenthrombose) in Verbindung gebracht.Diese Nebenwirkungen sind jedoch selten. In den meisten Fällen treten sie im ersten Jahr der Anwendung eines kombinierten hormonalen Kontrazeptivums auf.
- Wenn sich ein Blutgerinnsel in einer Bein- oder Fußvene bildet, kann dies eine tiefe Venenthrombose (TVT) verursachen.
- Wenn ein Blutgerinnsel aus dem Bein austritt und sich in der Lunge festsetzt, kann dies eine "Lungenembolie" verursachen.
- Sehr selten kann sich in einem anderen Organ wie dem Auge ein Gerinnsel bilden (Netzhautvenenthrombose).
Wann ist das Risiko, ein Blutgerinnsel in einer Vene zu entwickeln, am höchsten?
Das Risiko, ein Blutgerinnsel in einer Vene zu entwickeln, ist im ersten Jahr der erstmaligen Einnahme eines kombinierten hormonalen Kontrazeptivums am höchsten. Das Risiko kann noch höher sein, wenn Sie nach einer Pause von 4 oder mehr Wochen wieder ein kombiniertes hormonales Kontrazeptivum (das gleiche oder ein anderes Medikament) einnehmen.
Nach dem ersten Jahr ist das Risiko geringer, aber immer etwas höher als wenn Sie kein kombiniertes hormonales Kontrazeptivum anwenden.
Wenn Sie die Einnahme von Effiprev abbrechen, normalisiert sich Ihr Risiko, ein Blutgerinnsel zu entwickeln, innerhalb weniger Wochen.
Wie hoch ist das Risiko, ein Blutgerinnsel zu entwickeln?
Das Risiko hängt von Ihrem natürlichen VTE-Risiko und der Art des kombinierten hormonalen Kontrazeptivums ab, das Sie einnehmen.
Das Gesamtrisiko für die Entwicklung eines Blutgerinnsels im Bein oder in der Lunge (TVT oder LE) unter Effiprev ist gering.
- Von 10.000 Frauen, die kein kombiniertes hormonales Kontrazeptivum anwenden und nicht schwanger sind, entwickeln etwa 2 innerhalb eines Jahres ein Blutgerinnsel. Von 10.000 Frauen, die ein kombiniertes hormonales Kontrazeptivum anwenden, das Levonorgestrel, Norethisteron oder Norgestimat enthält, entwickeln etwa 5-7 pro Jahr ein Blutgerinnsel. -
- Es ist noch nicht bekannt, wie sich das Risiko der Bildung eines Blutgerinnsels unter Effiprev mit dem Risiko eines kombinierten hormonalen Kontrazeptivums, das Levonorgestrel enthält, vergleichen lässt.
- Das Risiko für die Bildung eines Blutgerinnsels hängt von Ihrer Krankengeschichte ab (siehe unter „Faktoren, die das Risiko für die Bildung eines Blutgerinnsels erhöhen“).
Faktoren, die das Risiko erhöhen, ein Blutgerinnsel in einer Vene zu entwickeln
Das Risiko, unter Effiprev ein Blutgerinnsel zu entwickeln, ist gering, kann jedoch unter bestimmten Bedingungen erhöht werden. Ihr Risiko ist größer:
- wenn Sie stark übergewichtig sind (Body-Mass-Index oder BMI über 30 kg/m2);
- wenn bei einem nahen Verwandten in jungen Jahren (unter etwa 50 Jahren) ein Blutgerinnsel im Bein, der Lunge oder einem anderen Organ aufgetreten ist. In diesem Fall könnten Sie eine erbliche Blutgerinnungsstörung haben;
- wenn Sie sich einer Operation unterziehen müssen oder aufgrund einer Verletzung oder Krankheit längere Zeit liegen müssen oder wenn Sie ein Bein in Gips haben. Möglicherweise müssen Sie die Einnahme von Effiprev einige Wochen vor der Operation oder während einer Operation abbrechen die Zeit, in der Sie weniger mobil sind Wenn Sie die Einnahme von Effiprev abbrechen müssen, fragen Sie Ihren Arzt, wann Sie mit der Einnahme wieder beginnen können;
- wenn Sie älter werden (insbesondere über 35 Jahre);
- wenn Sie vor weniger als ein paar Wochen entbunden haben.
Das Risiko, ein Blutgerinnsel zu entwickeln, steigt, je mehr Erkrankungen Sie haben. Flugreisen (Dauer > 4 Stunden) können das Risiko eines Blutgerinnsels vorübergehend erhöhen, insbesondere wenn Sie einige der anderen aufgeführten Risikofaktoren haben. Es ist wichtig, dass Sie Ihren Arzt informieren, wenn einer dieser Punkte auf Sie zutrifft, auch wenn Sie sich nicht sicher sind. Ihr Arzt wird möglicherweise entscheiden, dass Sie die Einnahme von Effiprev abbrechen.Wenn sich eine der oben genannten Bedingungen während der Anwendung von Effiprev ändert, zum Beispiel wenn ein naher Verwandter aus unbekannter Ursache eine Thrombose hat oder wenn Sie stark zunehmen, wenden Sie sich an Ihren Arzt.
BLUTGERINNSEL IN EINER ARTERIE
Was kann passieren, wenn sich in einer „Arterie“ ein Blutgerinnsel bildet?
Wie Blutgerinnsel in einer Vene können auch Blutgerinnsel in einer Arterie ernsthafte Probleme verursachen, zum Beispiel einen Herzinfarkt oder Schlaganfall.
Faktoren, die das Risiko erhöhen, ein Blutgerinnsel in einer Arterie zu entwickeln
Es ist wichtig zu beachten, dass das mit der Anwendung von Effiprev verbundene Herzinfarkt- oder Schlaganfallrisiko sehr gering ist, sich jedoch erhöhen kann:
- mit zunehmendem Alter (über 35 Jahre);
- wenn du rauchst. Bei der Anwendung eines kombinierten hormonalen Kontrazeptivums wie [Phantasiebezeichnung] wird empfohlen, mit dem Rauchen aufzuhören. Wenn Sie nicht in der Lage sind, mit dem Rauchen aufzuhören und über 35 Jahre alt sind, wird Ihr Arzt Ihnen möglicherweise raten, eine andere Art von Verhütungsmittel zu verwenden;
- wenn Sie übergewichtig sind;
- wenn Sie hohen Blutdruck haben;
- wenn ein Mitglied Ihrer unmittelbaren Familie in jungen Jahren (unter etwa 50 Jahren) einen Herzinfarkt oder Schlaganfall erlitten hat. In diesem Fall besteht möglicherweise auch ein hohes Risiko für einen Herzinfarkt oder Schlaganfall;
- wenn Sie oder ein naher Verwandter hohe Blutfettwerte (Cholesterin oder Triglyceride) haben;
- wenn Sie an Migräne leiden, insbesondere an Migräne mit Aura;
- wenn Sie Herzprobleme haben (Herzklappenfehler, eine Herzrhythmusstörung, die als Vorhofflimmern bezeichnet wird);
- wenn Sie Diabetes haben.
Wenn Sie an mehr als einer dieser Erkrankungen leiden oder wenn eine davon besonders schwerwiegend ist, kann das Risiko, ein Blutgerinnsel zu entwickeln, noch höher sein. Wenn sich eine der oben genannten Bedingungen während der Anwendung von Effiprev ändert, zum Beispiel wenn Sie mit dem Rauchen beginnen, wenn ein naher Verwandter aus unbekannter Ursache eine Thrombose hat oder wenn Sie stark zunehmen, wenden Sie sich an Ihren Arzt.
Schwangerschaft, Stillzeit und Fruchtbarkeit
Wenn Sie schwanger sind oder vermuten, schwanger zu sein, dürfen Sie Effiprev nicht einnehmen. Wenn während der Einnahme von Effiprev eine Schwangerschaft eintritt, sollte die Pille sofort abgesetzt werden. Die Anwendung von Effiprev während der Stillzeit kann das Volumen der Muttermilch verringern und die Zusammensetzung der Muttermilch verändern. Minimale Mengen an Wirkstoffen und/oder sonstigen Bestandteilen werden in die Muttermilch ausgeschieden, mit möglichen Auswirkungen Stillenden Müttern wird daher empfohlen, Effiprev nicht einzunehmen.Fragen Sie vor der Einnahme dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Effiprev hat keinen Einfluss auf das Führen von Fahrzeugen und den Gebrauch von Maschinen.
Effiprev enthält Lactose
Dieses Arzneimittel enthält Lactose, Glucose und (Soja-)Lecithin. Wenn Sie wissen, dass Sie gegen bestimmte Zucker, Erdnüsse oder Soja überempfindlich sind, sprechen Sie mit Ihrem Arzt, bevor Sie Effiprev einnehmen.
Dosierung und Art der Anwendung Wie ist Effiprev anzuwenden: Dosierung
Nehmen Sie Effiprev immer genau nach Absprache mit Ihrem Arzt oder Apotheker ein. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Jede Packung Effiprev enthält 21, 3 x 21,6 x 21, 13 x 21 Filmtabletten. Die Wochentage, an denen die Filmtabletten eingenommen werden sollen, sind auf der Verpackung angegeben.
Sie sollten versuchen, die Pille jeden Tag zur gleichen Zeit einzunehmen, wenn nötig mit Flüssigkeit. Nehmen Sie täglich eine Tablette in Pfeilrichtung ein, bis Sie die Packung aufgebraucht haben. Es folgen 7 Tage, in denen keine Pillen eingenommen werden. Während dieses 7-tägigen medikamentenfreien Intervalls sollte eine Entzugsblutung auftreten, in der Regel 2-3 Tage nach Einnahme der letzten Pille.
Beginnen Sie mit der nächsten Packung Effiprev am 8. Tag nach Einnahme der letzten Pille. Sie sollten mit der Einnahme der Tabletten aus der nächsten Packung Effiprev beginnen, auch wenn die Blutung noch andauert. Jede neue Packung wird am selben Wochentag begonnen wie früher, damit Sie sich leichter daran erinnern können, wann Sie die Tabletten wieder einnehmen müssen, und Ihr Zyklus wird immer an denselben Tagen des Monats stattfinden.
Wenn Sie die Anweisungen genau befolgen, kann die Pille Sie ab dem ersten Behandlungstag vor einer ungewollten Schwangerschaft schützen.
Einnahme der ersten Packung Effiprev
Keine hormonelle Verhütungsbehandlung im letzten Monat:
Eine Filmtablette, beginnend am ersten Tag Ihres Menstruationszyklus (der erste Tag Ihrer Periode, definiert als Tag 1), nehmen Sie die Pille mit dem richtigen Wochentag aus der Blisterpackung.
Umstellung von einem kombinierten Kontrazeptivum auf Effiprev (kombiniertes orales Kontrazeptivum, Vaginalring, transdermales Pflaster):
Die erste Filmtablette Effiprev sollte in den üblichen tablettenfreien Intervallen oder am ersten Tag unmittelbar nach Einnahme der letzten Tablette des vorherigen Verhütungsmittels (ohne „tablettenfreie“ Pause) eingenommen werden.
Wenn das zuvor eingenommene Produkt inaktive (hormonfreie) Tabletten enthielt, sollte die Einnahme von Effiprev mit der üblichen placebotablettenfreien Pause oder nach Einnahme der letzten aktiven (hormonhaltigen) Tablette des vorherigen Verhütungsmittels begonnen werden aktiv sind, fragen Sie Ihren Arzt oder Apotheker.
Wenn der Vaginalring oder das transdermale Pflaster bereits verwendet wurde, sollte Effiprev am Tag der Entfernung des Vaginalrings oder transdermalen Pflasters oder spätestens an dem Tag, an dem die neue Anwendung geplant ist, begonnen werden.
Wechsel von einer reinen Gestagen-Verhütungsmethode (Minipille):
Frauen, die reine Gestagen-Minipillen einnehmen, können jederzeit auf Effiprev umstellen, das am Tag nach Einnahme des vorherigen Verhütungsmittels (zur gewohnten Zeit) eingenommen werden kann. Eine zusätzliche Verhütungsmethode, zB Methoden, ist erforderlich 7 Tage nach Einnahme der Tabletten.
Wenn Sie zuvor empfängnisverhütende Injektionen oder empfängnisverhütende Implantate oder ein Gestagen-freisetzendes Intrauterinpessar (IUS) verwendet haben:
Diejenigen, die Implantate oder IUS verwenden, können am Tag der Entfernung des Implantats oder IUS beginnen. Frauen, die Injektionen erhalten, können mit der Einnahme der Filmtabletten am Tag der nächsten Injektion beginnen. Es ist notwendig, auf eine zusätzliche Verhütungsmethode zurückzugreifen, z. Barrieremethoden (prophylaktisch) innerhalb von 7 Tagen nach Einnahme der Tabletten.
Nach der Geburt eines Babys:
Wenn Sie gerade ein Baby bekommen haben, kann Ihr Arzt Ihnen empfehlen, Effiprev nach der Wiederaufnahme des ersten Menstruationszyklus einzunehmen. In einigen Fällen kann die hormonelle Empfängnisverhütung jedoch früher beginnen: Fragen Sie Ihren Arzt um Informationen. Wenn Sie Effiprev einnehmen, sollten Sie Ihr Baby nicht stillen, es sei denn, Ihr Arzt sagt Ihnen dies.
Nach einer Fehlgeburt oder Fehlgeburt: Befolgen Sie die Anweisungen Ihres Arztes.
Wenn Sie die Einnahme von Effiprev vergessen haben
Wenn die vergessene Tablette innerhalb von 12 Stunden eingenommen wird, sind keine weiteren Vorsichtsmaßnahmen erforderlich; die Tablette sollte eingenommen werden, sobald Sie sich daran erinnern, und die nachfolgenden Tabletten sollten zur gewohnten Zeit eingenommen werden Der empfängnisverhütende Schutz von Effiprev wird nicht beeinträchtigt.
Wenn die Einnahme der vergessenen Tablette länger als 12 Stunden dauert, wird der Verhütungsschutz verringert. Das Risiko einer ungewollten Schwangerschaft ist extrem hoch, wenn Sie die Einnahme der Pille zu Beginn oder am Ende der Packung vergessen.In diesem Fall sind folgende Regeln zu beachten
Wenn Sie in der ersten Woche vergessen haben, eine Tablette einzunehmen:
Sie muss die letzte vergessene Tablette einnehmen, auch wenn dies bedeutet, dass sie am selben Tag zwei Tabletten gleichzeitig einnehmen muss, und die Tabletten dann nach dem üblichen Schema weiter einnehmen.Zusätzliche empfängnisverhütende Maßnahmen (z Wenn Sie jedoch in den letzten sieben Tagen Geschlechtsverkehr hatten, kann eine Schwangerschaft nicht ausgeschlossen werden, in diesem Fall informieren Sie bitte ohne zu zögern Ihren Arzt.
Wenn Sie in der zweiten Woche vergessen haben, eine Tablette einzunehmen:
Sie müssen die letzte vergessene Tablette einnehmen, auch wenn dies bedeutet, dass Sie am selben Tag zwei Tabletten gleichzeitig einnehmen müssen, und dann die Tabletten nach dem üblichen Zeitplan weiter einnehmen.Wenn Sie die Tabletten in den letzten 7 Tagen regelmäßig eingenommen haben , müssen keine zusätzlichen Verhütungsmaßnahmen ergriffen werden.
Wenn Sie in Woche 3 vergessen haben, eine Tablette einzunehmen:
Bei Anwendung der folgenden Verfahren ist es nicht erforderlich, auf zusätzliche empfängnisverhütende Maßnahmen zurückzugreifen, solange die Tabletten in den letzten 7 Tagen regelmäßig eingenommen wurden.
Es gibt zwei mögliche Optionen:
- Sie muss die letzte vergessene Tablette einnehmen, auch wenn dies bedeutet, dass sie am selben Tag zwei Tabletten gleichzeitig einnehmen muss, und die Tabletten dann nach dem üblichen Zeitplan weiter einnehmen der nächste. Eine Entzugsblutung tritt wahrscheinlich erst am Ende der zweiten Packung auf, und Sie können an den Tabletteneinnahmetagen Schmierblutungen oder Entzugsblutungen bemerken.
- Die zweite Möglichkeit besteht darin, dass Sie die Einnahme der Tabletten aus der aktuellen Packung abbrechen, jedoch eine Einnahmepause von maximal sieben Tagen einhalten (die Tage, an denen die Tablette ausgelassen wurde, müssen gezählt werden) und dann mit einer neuen fortfahren Packung Wenn Sie die Packung am gewohnten Wochentag beginnen möchten, kann das „pillenfreie“ Intervall kürzer als 7 Tage sein!
Wenn Sie die Einnahme von mehr als einer Tablette vergessen haben:
Sprechen Sie mit Ihrem Arzt. Vergessen Sie nicht, dass in diesem Fall eine wirksame Verhütung nicht gewährleistet ist. Wenn mehrere Tabletten aus der aktuellen Packung vergessen wurden und im ersten tablettenfreien Intervall keine Abbruchblutung auftritt, ist die Wahrscheinlichkeit einer Schwangerschaft hoch. Es wird daher empfohlen, dass Sie Ihren Arzt kontaktieren, bevor Sie mit einer neuen Packung Effiprev beginnen.
Gastrointestinale Störungen
Wenn innerhalb von 3-4 Stunden nach Einnahme der Tablette Erbrechen oder starker Durchfall auftritt, wurde die Tablette möglicherweise nicht vollständig aus dem Magen-Darm-Trakt resorbiert. Diese Situation ähnelt der, wenn Sie vergessen haben, eine Tablette einzunehmen. In diesem Fall sollte eine Tablette so schnell wie möglich, möglicherweise innerhalb von 12 Stunden, eingenommen werden.
Wenn mehr als 12 Stunden vergangen sind, befolgen Sie die Anweisungen im Abschnitt „Wenn Sie die Einnahme von Effiprev vergessen haben“ bezüglich der Einnahme der vergessenen Tabletten.
Verzögern Sie die Periode der Menstruation
Es kann den Zeitpunkt des Einsetzens der Menstruation verzögern, wenn Sie Effiprev nach Beendigung der vorherigen Packung ohne Einhaltung des tablettenfreien Intervalls weiter einnehmen. Die Menstruation kann bis zum Ende der zweiten Packung oder, falls erforderlich, über einen längeren Zeitraum verschoben werden - kürzerer Zeitraum Während der Einnahme von Tabletten aus der zweiten Packung können an den Tabletteneinnahmetagen Schmierblutungen oder Abbruchblutungen auftreten. Nach Beendigung der zweiten Tablettenpackung kann die Einnahme von Effiprev nach einem tablettenfreien Zeitraum von 7 Tagen regelmäßig wieder aufgenommen werden.
Wenn Sie möchten, dass Ihre Periode an einem anderen Tag auftritt
Wenn Sie die Anweisungen zur Einnahme der Tabletten immer richtig befolgt haben, tritt Ihre Periode alle vier Wochen ungefähr am selben Tag ein.Wenn Sie möchten, dass Ihre Periode an einem anderen Wochentag beginnt, sollte die Länge des tablettenfreien Intervalls betragen nach Bedarf reduziert. Verlängern Sie niemals die tablettenfreie Zeit! Nehmen wir zum Beispiel an, dass Ihre Periode normalerweise am Freitag auftritt, aber Sie möchten, dass sie am Dienstag (also drei Tage früher) auftritt. Beginnen Sie dazu drei Tage früher mit der Einnahme der Tabletten aus der nächsten Packung. Wenn jedoch das Intervall ohne Tabletten stark verkürzt wird (3 Tage oder weniger), kommt es während der Einnahme der zweiten Packung nicht zu einer Blutstillung, sondern zu Schmier- oder Entzugsblutungen.
Was tun, wenn zwischen den Zyklen Blutungen auftreten?
In einigen Fällen können bei Frauen, die KOK einnehmen, kleine Entzugsblutungen oder Schmierblutungen auftreten, insbesondere in den ersten Monaten der Anwendung des Produkts. Es kann daher erforderlich sein, Tampons oder Damenbinden zu verwenden; Sie müssen die Pillen jedoch weiterhin einnehmen. Sobald sich Ihr Körper an die Wirkung der Filmtabletten gewöhnt hat, hören die unregelmäßigen Blutungen auf: Normalerweise dauert es drei Kurse, bis dies eintritt. Wenn die Blutung anhält, stärker erscheint oder wiederkehrt, wenden Sie sich an Ihren Arzt.
Was tun, wenn keine Entzugsblutung auftritt?
Wenn die Tabletten vorschriftsmäßig eingenommen wurden und kein Erbrechen oder Durchfall aufgetreten ist, ist eine Schwangerschaft sehr unwahrscheinlich. Sie sollten Effiprev wie gewohnt einnehmen. Wenn Ihre Periode nicht zweimal hintereinander auftritt, können Sie schwanger sein. Wenden Sie sich ohne zu zögern an Ihren Arzt. Sie können Effiprev nach einem Schwangerschaftstest auf Anraten Ihres Arztes weiter einnehmen.
Wenn Sie die Einnahme von Effiprev abbrechen
Sie können die Einnahme von Effiprev jederzeit beenden.Wenn Sie dennoch eine Schwangerschaft vermeiden möchten, fragen Sie Ihren Arzt nach anderen zuverlässigen Verhütungsmethoden.Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker.
Überdosierung Was ist zu tun, wenn Sie eine Überdosis Effiprev® eingenommen haben?
Wenn Sie eine größere Menge von Effiprev eingenommen haben, als Sie sollten
Es liegen keine Daten zur Überdosierung von Effiprev vor. Nach Informationen aus der Anwendung anderer kombinierter oraler Kontrazeptiva ist die Toxizität nach einer Überdosierung sowohl bei Erwachsenen als auch bei Kindern sehr gering. Eine Überdosierung kann Übelkeit, Erbrechen und bei Mädchen vaginale Blutungen verursachen. Wenn Sie bei Bedarf mehrere Tabletten von Effiprev eingenommen haben, fragen Sie Ihren Arzt um Rat.
Wenn Sie bemerkt haben, dass ein Kind wahrscheinlich mehrere Tabletten geschluckt hat, wenden Sie sich ohne zu zögern an Ihren Arzt.
Nebenwirkungen Was sind die Nebenwirkungen von Effiprev
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen. Wenn Sie Nebenwirkungen bemerken, insbesondere wenn diese schwerwiegend oder anhaltend sind, oder wenn sich Ihr Gesundheitszustand ändert, von dem Sie glauben, dass er auf Effiprev zurückzuführen ist, informieren Sie bitte Ihren Arzt.
Ein erhöhtes Risiko für die Entwicklung von Blutgerinnseln in den Venen (venöse Thromboembolien (VTE)) oder Blutgerinnseln in den Arterien (arterielle Thromboembolien (ATE)) besteht bei allen Frauen, die kombinierte hormonale Kontrazeptiva einnehmen. Ausführlichere Informationen zu den verschiedenen Risiken der Einnahme von kombinierten hormonalen Kontrazeptiva finden Sie in Abschnitt 2 „Was sollten Sie vor der Anwendung von Effiprev beachten?
Die Häufigkeit der Nebenwirkungen wurde wie folgt klassifiziert:
Frauen, die hormonelle Kontrazeptiva einnehmen, haben ein erhöhtes Risiko für Thromboembolien. Bestimmte Faktoren können dieses Risiko weiter erhöhen (siehe Abschnitt 2).
Schwere Nebenwirkungen
Zu schwerwiegenderen Nebenwirkungen bei Frauen, die kombinierte orale Kontrazeptiva einnehmen, siehe Abschnitt „Warnhinweise und Vorsichtsmaßnahmen“. Bei Bedarf sofort ärztliche Hilfe holen.
Andere mögliche Nebenwirkungen
In der folgenden Tabelle sind die Nebenwirkungen von Effiprev in absteigender Häufigkeit aufgelistet. Die angegebenen Häufigkeiten beziehen sich auf Nebenwirkungen, die möglicherweise im Zusammenhang mit Effiprev in klinischen Studien beobachtet wurden. Keine der Nebenwirkungen trat mit einer „sehr häufigen“ Häufigkeit auf.
Die Wahrscheinlichkeit, ein Blutgerinnsel zu entwickeln, kann höher sein, wenn Sie andere Erkrankungen haben, die dieses Risiko erhöhen (siehe Abschnitt 2 für weitere Informationen zu Erkrankungen, die das Risiko von Blutgerinnseln erhöhen und die Symptome eines Blutgerinnsels).
- Die folgenden Nebenwirkungen wurden bei Frauen beobachtet, die KOK einnahmen (siehe Abschnitt „Warnhinweise und Vorsichtsmaßnahmen“)
- Hypertonie;
- Lebertumore;
- gelblich-braune Flecken im Gesicht und am Körper (Chloasma);
- Entwicklung oder Verschlechterung von Krankheiten, deren Ursprung nicht vollständig geklärt ist, die aber mit der Anwendung kombinierter oraler Kontrazeptiva zusammenhängen:
- entzündliche Darmerkrankung (Morbus Crohn oder Colitis ulcerosa);
- Störung des Hämoglobinstoffwechsels (Porphyrie);
- einige Erkrankungen des Immunsystems (systemischer Lupus erythematodes);
- Hautausschlag mit Blasen im Endstadium der Schwangerschaft (Gestationsherpes);
- Krämpfe, Sydenhams Chorea;
- Blutgerinnungsstörung im Zusammenhang mit einer Nierenerkrankung (hämolytisch-urämisches Syndrom);
- hereditäres Angioödem;
- Gelbsucht.
Die Pille und Brustkrebs
Das Brustkrebsrisiko ist bei Frauen, die KOK einnehmen, etwas höher. Da das Risiko, an Brustkrebs zu erkranken, bei Frauen unter 40 Jahren jedoch gering ist, ist die Zahl der zusätzlichen Fälle im Vergleich zum Gesamtrisiko für Brustkrebs bescheiden. Sexualhormone beeinflussen die Brustdrüse. Variationen im hormonellen Bereich (zB durch die Anwendung hormoneller Kontrazeptiva) können Situationen schaffen, in denen die Empfindlichkeit der Brustdrüsen gegenüber anderen Faktoren, die die Tumorentstehung begünstigen, erhöht wird und damit die Wahrscheinlichkeit, an Krebs zu erkranken, steigt Die Entwicklung von Brustkrebs bei Frauen mittleren Alters hängt mit der frühen und umfangreichen Anwendung von KOK zusammen.
Wenn Sie eine der Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies gilt auch für Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker. Dies schließt alle Nebenwirkungen ein, die nicht in der Packungsbeilage beschrieben sind. Die Meldung dieser Auswirkungen kann auch über das National Reporting Network erfolgen. Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels bereitgestellt werden.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Verwenden Sie dieses Arzneimittel nicht nach dem auf der Packung und der Blisterpackung nach „Verwendbar bis“ angegebenen Verfallsdatum. Das Ablaufdatum bezieht sich auf den letzten Tag dieses Monats.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Werfen Sie Arzneimittel nicht in das Abwasser oder den Hausmüll. Fragen Sie Ihren Apotheker, wie Sie Arzneimittel, die Sie nicht mehr verwenden, entsorgen sollen. Dies trägt zum Schutz der Umwelt bei.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu haben, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS
EFFIPREV-TABLETTEN MIT FILM . BESCHICHTET
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Jede Filmtablette enthält 2 mg Dienogest und 0,03 mg Ethinylestradiol.
Hilfsstoffe mit bekannter Wirkung: Lactose-Monohydrat (54,6 mg), Glucose (0,085 mg) und Sojalecithin (0,031 mg).
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM
Filmtablette.
Weiße oder elfenbeinweiße, runde, bikonvexe Filmtabletten.
04.0 KLINISCHE INFORMATIONEN
04.1 Anwendungsgebiete
Hormonelle Verhütung.
Bei der Entscheidung, EFFIPREV zu verschreiben, müssen die aktuellen Risikofaktoren der einzelnen Frau berücksichtigt werden, insbesondere diejenigen im Zusammenhang mit venösen Thromboembolien (VTE) und der Vergleich zwischen dem mit EFFIPREV verbundenen VTE-Risiko und dem mit anderen kombinierten hormonellen Kontrazeptiva - KHK ( siehe Abschnitte 4.3 und 4.4).
04.2 Dosierung und Art der Anwendung
Dosierung
Die Filmtabletten sollten jeden Tag zur gleichen Zeit (ggf. mit Flüssigkeit) gemäß der auf der Blisterpackung angegebenen Reihenfolge eingenommen werden. An 21 aufeinanderfolgenden Tagen sollte täglich eine Filmtablette eingenommen werden. Jede weitere Packung sollte nach einer 7-tägigen tablettenfreien Zeit begonnen werden; Während dieser Zeit treten normalerweise Entzugsblutungen auf. Die Blutung beginnt normalerweise 2-3 Tage nach Einnahme der letzten Tablette und kann bei Einnahme der ersten Tablette aus der nächsten Packung noch andauern.
Art der Verabreichung
Zur oralen Anwendung
Wie beginnt man mit der Einnahme von Effiprev
Keine hormonelle Verhütungsbehandlung (im letzten Monat)
Die erste Filmtablette sollte am ersten Tag Ihres natürlichen Menstruationszyklus (am ersten Tag Ihrer Periode, definiert als Tag 1) eingenommen werden.
Umstellung von einem kombinierten Kontrazeptivum (KOK, Vaginalring, transdermales Pflaster) auf eine orale Kontrazeption
Die Frau sollte mit der Einnahme von Effiprev am Tag nach dem üblichen Tablettenintervall ohne Wirkstoff oder am Tag nach der letzten Placebotablette des vorherigen oralen Kontrazeptivums oder am Tag nach Einnahme der letzten aktiven Tablette des vorherigen oralen Kontrazeptivums beginnen oder transdermales Pflaster verwendet wurde, sollte die Frau mit der Einnahme von Effiprev vorzugsweise am Tag der Entfernung dieser Produkte oder spätestens bei der nächsten Anwendung beginnen.
Wechsel von einer reinen Gestagen-Verhütungsmethode (Minipille, Injektion, Implantat) oder von einem Gestagen freisetzenden Intrauterinpessar (IUS)
Frauen, die nur Gestagen-Minipillen einnehmen, können jederzeit auf KOK umsteigen. Diejenigen, die Implantate oder IUS verwenden, können am Tag der Entfernung des Implantats oder IUS beginnen. Frauen, die Injektionen erhalten, können mit der Einnahme der Filmtabletten am Tag der nächsten Injektion beginnen. In all diesen Fällen wird jedoch empfohlen, in den ersten 7 Tagen nach Einnahme der Tabletten eine zusätzliche unterstützende Verhütungsmethode anzuwenden.
Zur Stillzeit siehe Abschnitt 4.6.
Nach einer Abtreibung im ersten Trimester
Die Tabletten können sofort eingenommen werden; es sind keine zusätzlichen empfängnisverhütenden Maßnahmen erforderlich.
Nach der Geburt oder Abtreibung im zweiten Trimester
Die Einnahme der Tabletten kann 21-28 Tage nach der Entbindung oder nach einem Schwangerschaftsabbruch im zweiten Trimenon begonnen werden.Bei verzögerter Einnahme des Produktes muss bei den ersten auf eine zusätzliche Verhütungsmethode (zB Barrieremethode) zurückgegriffen werden. 7 Tage Einnahme der Tabletten. Wenn die Frau jedoch bereits Geschlechtsverkehr hatte, muss eine mögliche Schwangerschaft ausgeschlossen oder die erste Regelblutung abgewartet werden, bevor mit der Einnahme der Filmtabletten begonnen wird.
Verhalten bei vergessener Tablette
Wenn die vergessene Tablette innerhalb von 12 Stunden eingenommen wird, sind keine weiteren Vorsichtsmaßnahmen erforderlich; Die Tablette sollte eingenommen werden, sobald Sie sich daran erinnern, dass Sie sie vergessen haben, und die nachfolgenden Tabletten sollten zur gewohnten Zeit eingenommen werden.
Wenn Sie mit der Einnahme einer Tablette mehr als 12 Stunden zu spät kommen, kann der Verhütungsschutz herabgesetzt sein.In diesem Fall gelten die folgenden Grundsätze:
1. Die Tabletteneinnahme darf nie länger als 7 Tage unterbrochen werden.
2. Um eine "angemessene Unterdrückung der Hypothalamus-Hypophysen-Ovarial-Achse" zu erreichen, ist es notwendig, die Tabletten 7 Tage lang kontinuierlich einzunehmen.
Darauf aufbauend können folgende Vorschläge für die tägliche Praxis gemacht werden:
Erste Woche
Die Patientin sollte die letzte vergessene Tablette einnehmen, sobald sie sich daran erinnert, auch wenn es sich dabei um zwei Tabletten gleichzeitig handelt, und die Tabletten dann täglich zur gewohnten Zeit einnehmen. In den nächsten 7 Tagen sollten zusätzliche empfängnisverhütende Maßnahmen (z. B. Kondome) angewendet werden. Hatte die Frau jedoch in den letzten 7 Tagen Geschlechtsverkehr, kann eine Schwangerschaft nicht ausgeschlossen werden. Das Schwangerschaftsrisiko ist proportional zur Anzahl der vergessenen Tabletten und nimmt zu, wenn sich die Vergessensperiode dem monatlichen tablettenfreien Intervall nähert.
Zweite Woche
Die Patientin sollte die letzte vergessene Tablette einnehmen, sobald sie sich daran erinnert, auch wenn es sich dabei um zwei Tabletten gleichzeitig handelt, und die Tabletten dann täglich zur gewohnten Zeit einnehmen. Wenn die Frau die Tabletten in den 7 Tagen vor der vergessenen Tablette korrekt eingenommen hat, sind keine zusätzlichen empfängnisverhütenden Maßnahmen erforderlich. Wenn jedoch mehr als eine Tablette vergessen wurde oder die Tabletteneinnahme nicht regelmäßig erfolgt ist, sollten in den nächsten 7 Tagen zusätzliche empfängnisverhütende Maßnahmen ergriffen werden.
Dritte Woche
In diesem Zeitraum ist das Risiko einer verminderten Verhütungssicherheit angesichts des nahenden Intervalls ohne Tabletten extrem hoch. Es ist jedoch immer noch möglich, einen verminderten Verhütungsschutz durch eine Änderung des Tabletteneinnahmeplans zu verhindern. Bei Anwendung eines der folgenden Protokolle ist es daher nicht erforderlich, zusätzliche empfängnisverhütende Maßnahmen zu ergreifen, sofern die Frau in den 7 Tagen vor der ersten vergessenen Tablette alle Tabletten regelmäßig eingenommen hat. Wenn nicht, wird empfohlen, die erste der beiden Optionen zu befolgen und in den nächsten 7 Tagen zusätzliche empfängnisverhütende Maßnahmen zu ergreifen.
1.Die Patientin sollte die letzte vergessene Tablette einnehmen, sobald sie sich daran erinnert, auch wenn es sich dabei um zwei Tabletten gleichzeitig handelt, und die Tabletten dann täglich zur gewohnten Zeit einnehmen. Die nächste Packung sollte sofort nach Beendigung der aktuellen Packung begonnen werden, dh ohne Lücken zwischen den Packungen zu lassen. Es ist unwahrscheinlich, dass der Patient vor dem Ende der zweiten Packung eine Abbruchblutung verspürt, jedoch kann es bei der Einnahme von Tabletten zu Schmierblutungen oder -durchbrüchen kommen Blutung.
2. Die zweite Möglichkeit besteht darin, die Einnahme der Tabletten aus der aktuellen Packung abzubrechen und eine tablettenfreie Pause von bis zu sieben Tagen (einschließlich der Tage, an denen die Tabletten vergessen wurden) einzuhalten und dann mit einer neuen Packung fortzufahren.
Wenn viele Tabletten aus der aktuellen Packung vergessen wurden und im ersten regulären tablettenfreien Intervall keine Abbruchblutung auftritt, kann die Möglichkeit einer weiteren Schwangerschaft nicht ausgeschlossen werden.
Gastrointestinale Störungen
Wenn innerhalb von 3-4 Stunden nach Einnahme der Tablette Erbrechen oder Durchfall auftritt, wurde die Tablette möglicherweise nicht vollständig vom Körper aufgenommen.In diesem Fall sollte die Tablette so schnell wie möglich eingenommen werden.
Wenn mehr als 12 Stunden vergangen sind, befolgen Sie die Empfehlungen in Abschnitt 4.2 bezüglich des Weglassens einiger Tabletten Wenn der Patient das übliche Dosierungsschema nicht ändern möchte, muss die benötigte Tablette (oder Tabletten) aus einer neuen Packung entnommen werden.
So verschieben oder ändern Sie Ihre Widerrufsfrist
Um die Menstruation zu verzögern, muss Effiprev weiterhin eingenommen werden, indem nach Beendigung der vorherigen Packung von einer Packung zur anderen gewechselt wird, ohne das tablettenfreie Intervall einzuhalten. Während der Anwendung der zweiten Packung kann der Patient an den Tagen der Tabletteneinnahme Schmierblutungen oder Abbruchblutungen bemerken.Nach Beendigung der zweiten Tablettenpackung kann die Einnahme von Effiprev regelmäßig am Ende der üblichen 7-tägigen Pause wieder aufgenommen werden.
Wenn die Frau ihre Periode auf einen anderen Wochentag verschieben möchte, als es mit dem aktuellen Zeitplan der Fall ist, kann die Länge des tablettenfreien Intervalls auf die gewünschten Tage verkürzt werden , desto größer ist die Wahrscheinlichkeit von Schmierblutungen oder Entzugsblutungen während der Einnahme der zweiten Packung (ähnlich wie wenn Sie Ihre Periode verschieben möchten).
04.3 Kontraindikationen
Bei Vorliegen der folgenden Erkrankungen und Zustände ist die Anwendung kombinierter oraler Kontrazeptiva kontraindiziert: Beim erstmaligen Auftreten der unten aufgeführten Erkrankungen während der Anwendung der kombinierten Kontrazeptiva sollte die Einnahme sofort abgebrochen werden.
Kombinierte hormonale Kontrazeptiva (KOK) sollten unter den folgenden Bedingungen nicht angewendet werden:
- Vorhandensein oder Risiko einer venösen Thromboembolie (VTE)
• Venöse Thromboembolie – aktuelle (mit Einnahme von Antikoagulanzien) oder frühere VTE (z. B. tiefe Venenthrombose [TVT] oder Lungenembolie [LE])
• Bekannte erbliche oder erworbene Prädisposition für venöse Thromboembolien, wie Resistenz gegen aktiviertes Protein C (einschließlich Faktor-V-Leiden), Antithrombin-III-Mangel, Protein-C-Mangel, Protein-S-Mangel
• Größere Operation mit längerer Ruhigstellung (siehe Abschnitt 4.4)
• Hohes Risiko für venöse Thromboembolien aufgrund des Vorhandenseins mehrerer Risikofaktoren (siehe Abschnitt 4.4)
- Vorhandensein oder Risiko einer arteriellen Thromboembolie (ATE)
• Arterielle Thromboembolie – aktuelle oder frühere arterielle Thromboembolie (zB Myokardinfarkt) oder prodromale Erkrankungen (zB Angina pectoris)
• zerebrovaskuläre Erkrankung – aktueller oder früherer Schlaganfall oder prodromale Zustände (z. B. vorübergehende ischämische Attacke (vorübergehende ischämische Attacke, TIA))
• Bekannte erbliche oder erworbene Prädisposition für arterielle Thromboembolien, wie Hyperhomocysteinämie und Antiphospholipid-Antikörper (Anticardiolipin-Antikörper, Lupus-Antikoagulans)
• Migräne in der Anamnese mit fokalen neurologischen Symptomen
• Ein hohes Risiko für eine arterielle Thromboembolie aufgrund des Vorliegens mehrerer Risikofaktoren (siehe Abschnitt 4.4) oder des Vorliegens eines schwerwiegenden Risikofaktors wie:
- Diabetes mellitus mit Gefäßsymptomen
- schwerer Bluthochdruck
- schwere Dyslipoproteinämie
- Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile;
- aktuelles oder früheres zerebrovaskuläres Ereignis;
- schwere Lebererkrankung in der aktiven Phase oder in der Anamnese, wenn sich die Werte der Leberfunktionstests noch nicht normalisiert haben;
- Lebertumor in Aktion (gutartig oder bösartig) oder in der Anamnese;
- bekannte oder vermutete geschlechtssteroidabhängige Krebsarten (Krebse der Geschlechtsorgane oder der Brust);
- vaginale Blutung unbekannter Ursache;
- aktuelle oder frühere Pankreatitis, wenn sie mit schwerer Hypertriglyzeridämie einhergeht;
- schweres Nierenversagen oder akutes Nierenversagen.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung
Warnungen
Bei Vorliegen einer der unten aufgeführten Erkrankungen oder Risikofaktoren sollte die Eignung von EFFIPREV mit der Frau besprochen werden.
Im Falle einer Verschlechterung oder des erstmaligen Auftretens eines dieser Risikofaktoren oder Zustände sollte die Frau ihren Arzt konsultieren, um zu entscheiden, ob die Anwendung von EFFIPREV abgesetzt werden sollte.
Risiko einer venösen Thromboembolie (VTE)
Die Anwendung eines kombinierten hormonalen Kontrazeptivums (KOK) führt im Vergleich zur Nichtanwendung zu einem erhöhten Risiko für venöse Thromboembolien (VTE). Produkte, die Levonorgestrel, Norgestimat oder Norethisteron enthalten, sind mit einem geringeren Risiko für VTE verbunden Das mit EFFIPREV verbundene Risiko ist vergleichbar mit diesen Produkten mit geringerem Risiko. Die Entscheidung, ein anderes Produkt zu verwenden als ein Produkt, das mit einem niedrigeren VTE-Risiko verbunden ist, sollte nur nach Absprache mit der Frau getroffen werden, um sicherzustellen, dass sie das mit KHK verbundene VTE-Risiko versteht und wie seine aktuellen Risikofaktoren beeinflussen dieses Risiko und die Tatsache, dass das Risiko, eine VTE zu entwickeln, im ersten Jahr der Anwendung am höchsten ist.Es gibt auch Hinweise darauf, dass das Risiko steigt, wenn die Einnahme eines KOK nach einer Pause von 4 oder mehr wieder aufgenommen wird Wochen.
In Anbetracht der Möglichkeit schwerwiegender Gesundheitsschäden (siehe Abschnitt 4.8) ist es bei Fortbestehen von Risikofaktoren (wie Krampfadern, fortgeschrittener Venenentzündung und Thrombose, Vorliegen einer Herzerkrankung, Fettleibigkeit, Blutgerinnungsstörungen) erforderlich, sorgfältig über die möglichen Risiken und Vorteile der Anwendung kombinierter oraler Kontrazeptiva, bevor Sie mit der Behandlung mit Effiprev beginnen.
Etwa 2 von 10.000 Frauen, die kein KHK anwenden und nicht schwanger sind, entwickeln über einen Zeitraum von einem Jahr eine VTE. Bei einer alleinstehenden Frau kann das Risiko jedoch in Abhängigkeit von den zugrunde liegenden Risikofaktoren (siehe unten) viel höher sein.
Epidemiologische Studien bei Frauen, die niedrig dosierte kombinierte orale Kontrazeptiva anwenden (
Es wird geschätzt, dass von 10.000 Frauen, die ein levonorgestrelhaltiges KHK anwenden, etwa 61 in einem Jahr eine VTE entwickeln.
Begrenzte epidemiologische Daten legen nahe, dass das VTE-Risiko bei Dienogest-haltigen KOK dem Risiko bei Levonorgestrel-haltigen KOK ähnelt.
Die Zahl der VTE pro Jahr ist geringer als bei schwangeren oder postpartalen Frauen erwartet.
VTE kann in 1-2% der Fälle tödlich sein.
1 Medianwert im Bereich von 5–7 pro 10.000 Frauen/Jahr, basierend auf einem relativen Risiko von ca. 2,3–3,6 für Levonorgestrel enthaltende KOK im Vergleich zur Nichtanwendung.
Sehr selten wurde bei CHC-Anwendern über Thrombosen in anderen Blutgefäßen berichtet, z
Risikofaktoren für VTE
Das Risiko venöser thromboembolischer Komplikationen bei KHK-Anwenderinnen kann erheblich ansteigen, wenn zusätzliche Risikofaktoren vorliegen, insbesondere wenn mehr als ein Risikofaktor vorliegt (siehe Tabelle).
EFFIPREV ist kontraindiziert, wenn eine Frau mehrere Risikofaktoren aufweist, die ihr Risiko für eine Venenthrombose erhöhen (siehe Abschnitt 4.3). Hat eine Frau mehr als einen Risikofaktor, ist das erhöhte Risiko möglicherweise größer als die Summe der Einzelfaktoren, in diesem Fall sollte ihr Gesamtrisiko für eine VTE berücksichtigt werden , sollte ein KHK nicht verschrieben werden (siehe Abschnitt 4.3).
Tabelle: Risikofaktoren für VTE
Es besteht keine Einigkeit über die mögliche Rolle von Krampfadern und oberflächlicher Thrombophlebitis bei der Entstehung und dem Fortschreiten einer Venenthrombose.
Das erhöhte Thromboembolierisiko in der Schwangerschaft, insbesondere in der 6-wöchigen Phase des Wochenbetts, muss berücksichtigt werden (Informationen zu „Fruchtbarkeit, Schwangerschaft und Stillzeit“ siehe Abschnitt 4.6.
Symptome einer VTE (tiefe Venenthrombose und Lungenembolie)
Wenn Symptome dieser Art auftreten, sollten Frauen sofort einen Arzt aufsuchen und sie darüber informieren, dass sie ein KHK einnehmen.
Symptome einer tiefen Venenthrombose (TVT) können sein:
- einseitige Schwellung des Beins und / oder des Fußes oder entlang einer Beinvene;
- Schmerzen oder Druckempfindlichkeit im Bein, die nur beim Stehen oder Gehen zu spüren sind;
- erhöhtes Hitzegefühl im betroffenen Bein; Haut am Bein, die rot oder verfärbt ist.
Symptome einer Lungenembolie (LE) können sein:
- plötzliches und unerklärliches Auftreten von Kurzatmigkeit und schneller Atmung;
- plötzlicher Husten, der mit Hämoptyse verbunden sein kann;
- stechender Schmerz in der Brust;
- schwere Benommenheit oder Schwindel;
- schneller oder unregelmäßiger Herzschlag.
Einige dieser Symptome (wie „Atemnot“ und „Husten“) sind unspezifisch und können als häufigere oder weniger schwerwiegende Ereignisse fehlinterpretiert werden (z. B. Infektionen der Atemwege).
Andere Anzeichen eines Gefäßverschlusses können sein: plötzlicher Schmerz, Schwellung oder eine blassblaue Verfärbung einer „Extremität“.
Findet der Verschluss im Auge statt, können die Symptome von schmerzlosem Verschwommensehen bis hin zum Verlust des Sehvermögens reichen. Manchmal tritt der Sehverlust fast sofort auf.
Risiko einer arteriellen Thromboembolie (ATE)
Epidemiologische Studien haben die Anwendung von KHK mit einem erhöhten Risiko für arterielle Thromboembolien (Myokardinfarkt) oder zerebrovaskuläre Unfälle (z. B. transitorische ischämische Attacke, Schlaganfall) in Verbindung gebracht.Arterielle thromboembolische Ereignisse können tödlich sein.
Risikofaktoren von ATE
Das Risiko arterieller thromboembolischer Komplikationen oder eines zerebrovaskulären Unfalls bei KHK-Anwendern steigt bei Vorliegen von Risikofaktoren (siehe Tabelle). Effiprev ist kontraindiziert, wenn eine Frau einen schwerwiegenden Risikofaktor oder mehrere Risikofaktoren für eine ATE aufweist, die ihr Risiko für eine arterielle Thrombose erhöhen (siehe Abschnitt 4.3). Hat eine Frau mehr als einen Risikofaktor, kann es sein, dass die Risikoerhöhung größer ist als die Summe der Einzelfaktoren, in diesem Fall muss ihr Gesamtrisiko berücksichtigt werden. a CHC sollte nicht verschrieben werden (siehe Abschnitt 4.3).
Tabelle: Risikofaktoren von ATE
Symptome von ATE
Wenn Symptome dieser Art auftreten, müssen Frauen Wenden Sie sich sofort an einen Arzt und informieren Sie ihn, dass Sie ein KHK einnehmen.
Symptome eines zerebrovaskulären Unfalls können sein:
- plötzliches Taubheitsgefühl oder Schwäche im Gesicht, Arm oder Bein, insbesondere auf einer Körperseite;
- plötzliche Schwierigkeiten beim Gehen, Schwindel, Gleichgewichts- oder Koordinationsverlust;
- plötzliche Verwirrung, Schwierigkeiten beim Sprechen oder Verstehen;
- plötzliche Schwierigkeiten beim Sehen auf einem oder beiden Augen;
- plötzliche, schwere oder anhaltende Migräne ohne bekannte Ursache;
- Bewusstlosigkeit oder Ohnmacht mit oder ohne Krämpfe.
Vorübergehende Symptome deuten darauf hin, dass es sich um eine transitorische ischämische Attacke (TIA) handelt.
Symptome eines Myokardinfarkts (MI) können sein:
- Schmerzen, Unwohlsein, Druck, Schweregefühl, Quetsch- oder Völlegefühl in Brust, Arm oder unterhalb des Brustbeins;
- in Rücken, Kiefer, Hals, Arme, Bauch ausstrahlende Beschwerden;
- Völlegefühl, Verdauungsstörungen oder Erstickungsgefühl;
- Schwitzen, Übelkeit, Erbrechen oder Schwindel;
- extreme Schwäche, Angst oder Kurzatmigkeit;
- schneller oder unregelmäßiger Herzschlag.
Tumore
In einigen Studien wurde bei Frauen unter Langzeitbehandlung mit KOK über ein erhöhtes Risiko für Gebärmutterhalskrebs berichtet; es bleibt jedoch umstritten, inwieweit dieses Ergebnis auf die verwirrenden Effekte für die Interpretation des Ergebnisses selbst (wie Sexualverhalten, Inzidenz einer humanen Papillomavirus-Infektion etc.) zurückzuführen ist.
Eine Metaanalyse von 54 epidemiologischen Studien ergab, dass bei Frauen, die derzeit KOK anwenden, ein leicht erhöhtes relatives Risiko (RR = 1,24) für die Brustkrebsdiagnose besteht. Dieses zusätzliche Risiko nimmt über 10 Jahre nach Absetzen der KOK-Behandlung ab.Weitere Informationen siehe Abschnitt 4.8.
Brustkrebs gehört zur Familie der hormonabhängigen bösartigen Tumoren. Einige Erkrankungen wie frühe Menarche, späte Menopause (nach 52 Jahren), Nulliparität, das Vorhandensein anovulatorischer Zyklen usw. sind seit langem als Risikofaktoren für die Entwicklung von Brustkrebs anerkannt. Diese Risikofaktoren erhöhen die Möglichkeit hormoneller Effekte bei der Pathogenese von Brustkrebs. Hormonrezeptoren spielen eine zentrale Rolle in der Biologie von Brustkrebs. Einige dieser Hormonrezeptoren induzieren Wachstumsfaktoren wie den transformierenden Wachstumsfaktor Alpha (TGF-Alpha).
Östrogen und Gestagen beeinflussen die Vermehrung von Brustkrebszellen. Dies stellt unter anderem die biologische Begründung für die pharmakologische Behandlung von postmenopausalem Hormonrezeptor-positivem Brustkrebs dar.
Zahlreiche epidemiologische Studien zum Zusammenhang zwischen der Anwendung kombinierter oraler Kontrazeptiva und Brustkrebs erkennen, dass die Entstehung von Brustkrebs bei Frauen mittleren Alters mit der frühen und umfassenden Anwendung kombinierter oraler Kontrazeptiva zusammenhängt. Dies ist jedoch nur ein Faktor unter den möglichen Faktoren.
In seltenen Fällen wurden bei Frauen, die orale Langzeitkontrazeptiva eingenommen hatten, gutartige und sehr selten bösartige Lebertumore beobachtet. In Einzelfällen führten diese Tumoren zu lebensbedrohlichen Bauchblutungen. Bei starken Schmerzen im Oberbauch, Hepatomegalie oder Anzeichen einer intraabdominalen Blutung sollte differenzialdiagnostisch an die Möglichkeit einer hepatischen Neoplasie gedacht werden.
Andere Bedingungen
Wenn in der persönlichen oder familiären Vorgeschichte des Patienten eine Hypertriglyzeridämie vorliegt, kann die Anwendung von KOK das Risiko einer Pankreatitis erhöhen.
Obwohl ein erhöhter Blutdruck bei Frauen, die KOK einnehmen, häufig auftritt, stellen klinisch relevante Blutdruckerhöhungen ein seltenes Ereignis dar. Wenn sich jedoch während der Einnahme von KOK eine Hypertonie entwickelt, sollte die Behandlung abgebrochen und eine geeignete antihypertensive Therapie eingeleitet werden. Nach erfolgreicher Auflösung des Bluthochdrucks kann die Behandlung mit kombinierten oralen Kontrazeptiva wieder aufgenommen werden, wenn der Arzt dies für klinisch angemessen hält.
Wenn während der Anwendung eines KOK bei Vorliegen eines vorbestehenden hypertensiven Zustandes durchweg erhöhte Blutdruckwerte oder ein deutlicher Blutdruckanstieg beobachtet werden, die nicht ausreichend auf eine antihypertensive Behandlung ansprechen, sollte das KOK abgesetzt werden.
Gegebenenfalls kann die Anwendung von KOK wieder aufgenommen werden, wenn nach einer antihypertensiven Therapie normotonische Werte aufgezeichnet werden.
Obwohl kein kausaler Zusammenhang nachgewiesen wurde, verschlechtern sich die folgenden Krankheiten / Zustände sowohl bei der Anwendung von KOK als auch bei einer Schwangerschaft: cholestatischer Ikterus und / oder cholestatischer Pruritus, Gallensteine, Porphyrie, systemischer Lupus erythematodes, hämolytisch-urämisches Syndrom, Sydenham-Chorea, Herpes während der Schwangerschaft, verursachte Schwerhörigkeit durch Otosklerose des Mittelohrs.
Bei Vorliegen einer aktiven oder chronischen Lebererkrankung sollte die Anwendung von KOK ausgesetzt werden, bis sich die Leberfunktionstests wieder normalisiert haben.
Das Wiederauftreten von cholestatischer Gelbsucht und/oder Juckreiz, die sich bereits in der Schwangerschaft oder während einer früheren Behandlung mit Sexualsteroiden manifestiert haben, erfordert das Absetzen hormoneller Kontrazeptiva.
KOK können die Glukosetoleranz verringern und den Bedarf an Insulin in peripheren Geweben erhöhen; Bei Frauen, die KOK einnehmen, ist es jedoch normalerweise nicht erforderlich, das Antidiabetikum zu ändern. Allerdings sollten Frauen mit Diabetes sorgfältig überwacht werden, insbesondere zu Beginn der Einnahme der Tabletten.
Chloasma kann gelegentlich auftreten, insbesondere bei Frauen mit Chloasma gravidarum in der Vorgeschichte. Frauen mit einer Neigung zu Chloasma sollten während der Einnahme dieses Arzneimittels Sonnen- oder UV-Strahlung vermeiden.
Bei Frauen mit hereditärem Angioödem können exogene Östrogene die Symptome eines Angioödems auslösen oder verschlimmern.
Während der Anwendung von KOK wurde über eine Verschlechterung einer endogenen Depression oder Epilepsie berichtet.
Die Anwendung von Östrogen bei Mädchen kann zu einem vorzeitigen Verschluss der Epiphyse mit einer daraus resultierenden Verringerung der Endgröße im Erwachsenenalter führen.
Verbindungen, die Gestagene enthalten, können die antagonistischen Eigenschaften von Aldosteron aufweisen, die einen großen Einfluss auf den Kaliumspiegel haben können.
Ärztliche Untersuchungen / Besuche
Vor Beginn oder Wiederaufnahme der Anwendung von Effiprev sollte eine vollständige Anamnese (einschließlich Familienanamnese) erhoben und eine Schwangerschaft ausgeschlossen, der Blutdruck gemessen und eine klinische Untersuchung unter Berücksichtigung von Kontraindikationen durchgeführt werden (siehe Abschnitt 4.3) und Warnhinweise (siehe Abschnitt 4.4) Es ist wichtig, eine Frau auf Informationen in Bezug auf venöse oder arterielle Thrombosen aufmerksam zu machen, einschließlich des mit Effiprev im Vergleich zu anderen KHK verbundenen Risikos, Symptome von VTE und ATE, bekannte Risikofaktoren und was in Fällen zu tun ist bei Verdacht auf Thrombose.
Die Frau sollte auch auf die Notwendigkeit hingewiesen werden, die Packungsbeilage sorgfältig zu lesen und deren Ratschläge zu befolgen. Häufigkeit und Art der Untersuchungen sollten sich an etablierten Richtlinien orientieren und an die jeweilige Frau angepasst werden.
Frauen sollten darauf hingewiesen werden, dass hormonelle Verhütungsmittel nicht vor HIV-Infektionen (AIDS) und anderen sexuell übertragbaren Krankheiten schützen.
Regelmäßige regelmäßige ärztliche Kontrollen sind wichtig, da einige Kontraindikationen oder Risikofaktoren erst während der Anwendung von KOK auftreten können.
Reduzierte Wirksamkeit
Die Wirksamkeit von KOK kann unter folgenden Umständen verringert sein: wenn der Patient die Tabletten nicht regelmäßig einnimmt, bei Erbrechen oder schwerem Durchfall (siehe Abschnitt 4.2) oder aufgrund von Wechselwirkungen mit anderen Arzneimitteln (siehe Abschnitt 4.5).
Anomalien der Zyklussteuerung
Die Einnahme von oralen Kontrazeptiva kann insbesondere in den ersten Monaten der Anwendung zu unregelmäßigen vaginalen Blutungen (Schmier- oder Abbruchblutungen) führen. Daher ist es ratsam, einen unregelmäßigen Blutverlust erst nach Erreichen eines Hormonhaushalts zu beurteilen, der in der Regel nach drei Behandlungen auftritt Fahrräder.
Bei anhaltenden unregelmäßigen Blutungen oder nach zuvor regelmäßigen Zyklen sind mögliche nicht-hormonelle Ursachen auszuschließen und geeignete diagnostische Maßnahmen, einschließlich ggf. diagnostischer Kürettage, zum Ausschluss einer Malignität oder Schwangerschaft durchzuführen.
Gelegentlich treten Entzugsblutungen während der freien Tage überhaupt nicht auf. Wenn die Tabletten richtig eingenommen wurden (gemäß den Anweisungen in Abschnitt 4.2), ist es sehr unwahrscheinlich, dass Sie schwanger sind. Wenn am Ende der zweiten Tablettenpackung keine Abbruchblutung auftritt oder die Frau die oben genannten Ratschläge nicht befolgt hat, muss eine Schwangerschaft vor Beginn einer neuen Packung ausgeschlossen werden.
Metabolische Wechselwirkungen, die zu einer erhöhten Clearance von Sexualhormonen führen, können Entzugsblutungen auslösen oder die empfängnisverhütende Wirkung verringern (siehe Abschnitt 4.5).
Pflanzliche Zubereitungen, die Johanniskraut (Hypericum perforatum) enthalten, sollten nicht gleichzeitig mit Effiprev eingenommen werden, da sie zu einer potenziellen Verringerung der empfängnisverhütenden Wirksamkeit führen können (siehe Abschnitt 4.5).
Effiprev enthält Lactose, Glucose und Lecithin (aus Soja). Patienten mit der seltenen hereditären Galactose-Intoleranz, Lapp-Lactase-Mangel, Glucose-Galactose-Malabsorption oder Erdnuss- und Sojaallergie sollten dieses Arzneimittel nicht einnehmen.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Wechselwirkungen mit anderen Arzneimitteln
Mehrere Arzneimittel, die die Clearance von Sexualhormonen erhöhen, können Entzugsblutungen auslösen oder die empfängnisverhütende Wirkung herabsetzen.Diese Wechselwirkungen wurden bei Hydantoin, Barbituraten, Primidon, Carbamazepin und Rifampicin nachgewiesen.Ein Wechselwirkung wird auch bei Rifabutin, Efavirenz, Nevirapin, Oxycarbazepin, Topiramat, Felbamat, Ritonavir, Nelvinafir, Griseofulvin und Johanniskraut enthaltende pflanzliche Präparate (Hypericum perforatum) Diese Arzneimittel erhöhen die Induktion von Leberenzymen.
Auch bei einigen Antibiotika (z. B. Ampicillin oder Tetracyclin) ist eine Verringerung der Wirksamkeit von KOK möglich, wobei der Mechanismus dieser Wirkung noch nicht aufgeklärt ist.
Frauen, die eine Kurzzeittherapie (bis zu einer Woche) mit einer der oben genannten Arzneimittelklassen erhalten, müssen während der gleichzeitigen Einnahme des Arzneimittels und 7 Tage nach Beendigung des Arzneimittels zusätzliche empfängnisverhütende Maßnahmen (z. B. eine Barrieremethode) anwenden.
Die gleichzeitige Behandlung mit Rifampicin erfordert die Anwendung zusätzlicher empfängnisverhütender Maßnahmen (z. B. eine Barrieremethode) während der Einnahme des gleichzeitigen Arzneimittels und für 4 Wochen nach dessen Absetzen. Wenn die gleichzeitige Anwendung des Arzneimittels auch nach dem Ende einer Packung fortgesetzt wird, sollte mit der nächsten Packung desselben begonnen werden, ohne das übliche Intervall ohne Einnahme einzuhalten.
Bei einer Langzeitbehandlung mit Leberenzyminduktoren sollte die Dosis der empfängnisverhütenden Steroide erhöht werden. Wenn die hohe Dosierung Nebenwirkungen (z. B. unregelmäßige Blutungen) verursacht oder unwirksam erscheint, sollte eine andere nicht-hormonelle Verhütungsmethode angewendet werden.
Bekannte Inhibitoren des CYP3A4-Enzyms wie Azol-Antimykotika, Cimetidin, Verapamil, Makrolide, Diltiazem, Antidepressiva und Grapefruitsaft können die Plasmaspiegel von Dienogest erhöhen.
Orale Kontrazeptiva können den Stoffwechsel anderer Arzneimittel beeinträchtigen. Folglich können Plasma- und Gewebekonzentrationen erhöht (z. B. Ciclosporin) oder erniedrigt (z. B. Lamotrigin) sein.
Die Gestagenverbindung kann mit ACE-Hemmern, Angiotensin-II-Rezeptor-Antagonisten, kaliumsparenden Diuretika, Aldosteron-Antagonisten und nicht-steroidalen entzündungshemmenden Arzneimitteln interagieren.
Im Studium in vitro dienogest hemmte die Funktion des Cytochrom-P450-Enzymsystems bei der verwendeten Dosis nicht, daher sind Wechselwirkungen mit diesem Enzymsystem nicht denkbar.
Labortests
Die Anwendung von empfängnisverhütenden Steroiden kann die Ergebnisse einiger Labortests beeinflussen, einschließlich biochemischer Parameter der Leber-, Schilddrüsen-, Nebennieren- und Nierenfunktion, Plasmaproteinspiegel (wie Kortikosteroid-bindendes Globulin) und Lipidfraktionen/Lipoprotein, Glukosestoffwechselparameter und die von Gerinnung und Fibrinolyse Diese Schwankungen bleiben jedoch im Normbereich.
Notiz: Informationen zur Fachinformation von Begleitmedikationen sollten zu Rate gezogen werden, um mögliche Wechselwirkungen zu identifizieren.
04.6 Schwangerschaft und Stillzeit
Schwangerschaft
Effiprev ist während der Schwangerschaft nicht indiziert.
Wenn während der Einnahme des oralen Kontrazeptivums eine Schwangerschaft eintritt, sollte die Behandlung sofort abgebrochen werden Umfangreiche epidemiologische Studien haben weder ein erhöhtes Risiko für angeborene Fehlbildungen bei Kindern von Frauen gezeigt, die vor der Schwangerschaft orale Kontrazeptiva eingenommen hatten, noch wurden teratogene Wirkungen auf die Nachkommen festgestellt, wenn das Arzneimittel wurde in den frühen Stadien der Schwangerschaft eingenommen. Diese Studien wurden nicht mit Effiprev durchgeführt.
Da nur begrenzte Daten zur Anwendung von Effiprev während der Schwangerschaft vorliegen, können keine Schlussfolgerungen zu unerwünschten Wirkungen auf die Schwangerschaft oder die Gesundheit des Fötus oder Neugeborenen gezogen werden.
Tierexperimentelle Studien haben eine Reproduktionstoxizität während der Schwangerschaft und Stillzeit gezeigt (siehe Abschnitt 5.3) Auswirkungen auf den Menschen sind nicht bekannt. Basierend auf den vorliegenden Studien zur Anwendung oraler Kontrazeptiva während der Schwangerschaft gibt es keine Hinweise auf mögliche teratogene Wirkungen.
Das erhöhte Thromboembolierisiko in der postpartalen Phase sollte berücksichtigt werden, wenn die Einnahme von Effiprev wieder aufgenommen wird (siehe Abschnitte 4.2 und 4.4).
Fütterungszeit
Die Einnahme von KOK während der Stillzeit kann die Menge reduzieren und die Zusammensetzung der Muttermilch verändern. Minimale Mengen an Wirkstoffen und/oder Hilfsstoffen werden in die Muttermilch ausgeschieden, mit möglichen Auswirkungen auf das Neugeborene. Stillenden Müttern wird daher empfohlen, Effiprev nicht einzunehmen.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Es wurden keine Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen beobachtet.
04.8 Nebenwirkungen
Beschreibung einiger Nebenwirkungen
Bei KHK-Anwenderinnen wurde ein erhöhtes Risiko für arterielle und venöse thrombotische und thromboembolische Ereignisse, einschließlich Myokardinfarkt, Schlaganfall, transitorische ischämische Attacken, Venenthrombose und Lungenembolie, beobachtet und dieses Risiko wird in Abschnitt 4.4 ausführlicher erörtert.
Die folgende Tabelle listet die Nebenwirkungen von Tabletten mit 2 mg Dienogest / 0,03 mg Ethinylestradiol in absteigender Häufigkeit auf. Diese Häufigkeiten stehen im Zusammenhang mit Nebenwirkungen, die in klinischen Studien mit Dienogest 2 mg / Ethinylestradiol 0,03 mg Tabletten beobachtet wurden (insgesamt nahmen 3590 Frauen an diesen Studien teil); das Auftreten dieser Nebenwirkungen kann mit der Anwendung von Effiprev zusammenhängen. Da alle Nebenwirkungen mit einer Häufigkeit von weniger als 1/10 auftraten, wurde keine von ihnen als „sehr häufig“ eingestuft.
Nebenwirkungen wurden nach der folgenden Häufigkeitskonvention klassifiziert:
Sehr häufig (≥ 1/10)
Häufig (≥ 1/100 bis
Gelegentlich (≥ 1 / 1.000 bis
Selten (≥ 1 / 10.000a
Sehr selten (
Die folgenden Nebenwirkungen wurden in Studien mit Effiprev mit 2 mg Dienogest / 0,03 mg Ethinylestradiol berichtet:
Die folgenden Nebenwirkungen wurden bei Frauen, die KOK einnahmen, berichtet:
- venöse oder arterielle Thromboembolie
- zerebrovaskuläre Ereignisse;
- Bluthochdruck;
- Lebertumoren;
- Entwicklung oder Verschlimmerung von Vorerkrankungen nach der Anwendung kombinierter oraler Kontrazeptiva, wie Morbus Crohn, Colitis ulcerosa, Porphyrie, systemischer Lupus erythematodes, Herpes Gestationsherpes, Sydenham-Chorea, hämolytisch-urämisches Syndrom, cholestatischer Ikterus;
- chloasma.
Bei Frauen, die KOK einnehmen, besteht ein leicht erhöhtes Brustkrebsrisiko. Da das Risiko, an Brustkrebs zu erkranken, bei Frauen unter 40 Jahren jedoch gering ist, ist die Zahl der zusätzlichen Fälle im Vergleich zum Gesamtrisiko für Brustkrebs bescheiden. Weitere Informationen finden Sie in den Abschnitten 4.3 und 4.4.
Bei Frauen mit hereditärem Angioödem können exogene Östrogene die Symptome eines Angioödems auslösen oder verschlimmern.
Weitere Informationen finden Sie in den Abschnitten 4.3 und 4.4.
Meldung vermuteter Nebenwirkungen
Es ist wichtig, vermutete Nebenwirkungen nach der Zulassung des Arzneimittels zu melden. Dies ermöglicht eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels Angehörige von Gesundheitsberufen sollten jeden Verdachtsfall einer Nebenwirkung über das National Reporting Network melden.
04.9 Überdosierung
Die akute orale Toxizität von Dienogest und Ethinylestradiol ist gering. Wenn ein kleines Kind eine beträchtliche Menge Effiprev einnimmt, verringert sich die Wahrscheinlichkeit, toxische Symptome zu entwickeln. Symptome, die bei einer Überdosierung auftreten können, sind Übelkeit, Erbrechen und bei jungen Mädchen Entzugsblutungen. Es ist keine besondere Behandlung erforderlich. Bei Bedarf kann eine symptomatische Behandlung erfolgen.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN
05.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Gestagene und Östrogene, fixe Kombination.
ATC-Code: G03AA.
Effiprev ist ein kombiniertes orales Kontrazeptivum mit antiandrogener Wirkung, das Ethinylestradiol als Östrogen und Dienogest als Gestagen enthält.
Wirkmechanismus
Die empfängnisverhütende Wirkung von Effiprev beruht auf dem Zusammenwirken mehrerer Faktoren, von denen die wichtigsten die Hemmung des Eisprungs und Veränderungen des Zervixschleims sind.
Ethinylestradiol ist ein starkes, oral wirksames synthetisches Östrogen. Wie natürliches Estradiol hat Ethinylestradiol eine proliferative Wirkung in den Epitheln der weiblichen Geschlechtsorgane. Es stimuliert die Produktion von Zervixschleim, reduziert dessen Viskosität und erhöht seine Faserigkeit. L "Ethinylestradiol fördert das Wachstum von Milchgänge und hemmt das Stillen." Ethinylestradiol stimuliert die extrazelluläre Wasserretention. Ethinylestradiol beeinflusst die Parameter des Lipid- und Kohlenhydratstoffwechsels, der Hämostase, des Renin-Angiotensin-Aldosteron-Systems und der Proteinbindung.
Dienogest ist ein Derivat von Nortestosteron, das in vitro eine 10-30 mal geringere Affinität zu Progesteronrezeptoren aufweist als andere synthetische Gestagene. In vivo dienogest zeigte keine signifikanten androgenen, mineralokortikoiden oder glukokortikoiden Wirkungen.
Als Monotherapie verabreicht, hemmt Dienogest den Eisprung bei einer Dosis von 1 mg / Tag.
05.2 Pharmakokinetische Eigenschaften
Ethinylestradiol
Absorption
Oral eingenommenes Ethinylestradiol wird schnell und vollständig resorbiert Nach der Einnahme von Effiprev werden maximale Serumkonzentrationen von ca. 67 pg/ml in 1,5-4 Stunden erreicht. Nach „Resorption“ und „First-Pass-Effekt“ wird Ethinylestradiol weitgehend metabolisiert, mit einer mittleren oralen Bioverfügbarkeit von ca. 44 %.
Verteilung
Ethinylestradiol bindet stark, aber nicht spezifisch an Serumalbumin (ca. 98%) und erhöht die Serumspiegel des Steroidhormon-bindenden Globulins (SHBG). Ethinylestradiol hat ein scheinbares Verteilungsvolumen von ca. 2,8–8,6 l/kg.
Biotransformation
Ethinylestradiol wird sowohl in der Dünndarmschleimhaut als auch in der Leber konjugiert. Ethinylestradiol wird durch aromatische Hydroxylierung metabolisiert, jedoch werden verschiedene Arten von hydroxylierten und methylierten Metaboliten erzeugt, die als freie Metabolite oder als Glucuronid- oder Sulfatkonjugate vorliegen Die metabolische Clearance-Rate beträgt ungefähr 2,3-7 ml / min / kg.
Beseitigung
Die Serumspiegel von Ethinylestradiol werden nach zwei verschiedenen kinetischen Phasen reduziert, die durch Halbwertszeiten von 1 Stunde und 10-20 Stunden gekennzeichnet sind. Unverändertes Arzneimittel unterliegt keiner Ausscheidung. Die Metaboliten von Ethinylestradiol werden mit dem Urin und der Galle mit einem Verhältnis von 4:6 und einer Halbwertszeit von ungefähr 1 Tag ausgeschieden.
Gleichgewichtszustand
Der Steady-State wird in der zweiten Hälfte der Behandlungszeit erreicht, wenn der Serumspiegel den doppelten Wert einer Einzeldosis beträgt.
Dienogest
Absorption
Oral eingenommenes Dienogest wird schnell und vollständig resorbiert. Nach Einnahme von Effiprev werden in 2,5 Stunden maximale Serumkonzentrationen von ca. 51 pg/ml erreicht, in Verbindung mit Ethinylestradiol beträgt die durchschnittliche Bioverfügbarkeit ca. 96 %.
Verteilung
Dienogest bindet an Serumalbumin, aber nicht an SHBG oder Corticosteroid-bindendes Globulin (CBG).10 % der im Serum vorhandenen Dienogest-Menge sind freies Steroid, während 90 % unspezifisch an Albumin gebunden sind.
Dienogest hat ein scheinbares Verteilungsvolumen von ca. 37-45 l.
Biotransformation Dienogest wird hauptsächlich über Hydroxylierung metabolisiert; Konjugation spielt jedoch auch eine wichtige Rolle bei der Bildung von endokrinologisch inaktiven Metaboliten. Diese Metaboliten werden schnell aus dem Plasma eliminiert, so dass außer dem unveränderten Anteil von Dienogest keine signifikanten Mengen seiner Metaboliten im menschlichen Plasma nachweisbar sind. Die Gesamtclearance (Cl / F) nach der Verabreichung einer Einzeldosis beträgt 3,6 l / Stunde.
Beseitigung
Dienogest hat eine "Halbwertszeit von 8,5-10,8 Stunden. Nur vernachlässigbare Mengen von Dienogest werden unverändert über die Niere ausgeschieden. Nach Verabreichung einer Dosis von 0,1 mg/kg beträgt das Verhältnis von renaler zu fäkaler Ausscheidung 3:1. Nach oraler Gabe werden 86 % der Dosis innerhalb von 6 Tagen eliminiert; ein beträchtlicher Teil wird in den ersten 24 Stunden hauptsächlich mit dem Urin ausgeschieden.
Gleichgewichtszustand
Das pharmakokinetische Profil von Dienogest wird durch den SHBG-Spiegel im Serum nicht beeinflusst. Bei täglicher Einnahme werden die Serumspiegel von Dienogest um das Eineinhalbfache erhöht und der Steady State wird nach 4 Tagen erreicht.
05.3 Präklinische Sicherheitsdaten
In Tierversuchen wurde beobachtet, dass die Wirkung von Ethinylestradiol und Dienogest auf die pharmakologischen Eigenschaften der Wirkstoffe beschränkt ist.
Studien zur Reproduktionstoxizität, die mit Dienogest durchgeführt wurden, haben die typischen Wirkungen von Gestagenen gezeigt: vermehrte Anomalien vor und nach der Einnistung, Verlängerung der Trächtigkeitsdauer, erhöhte neonatale Sterblichkeit bei Welpen. Die Verabreichung einer hohen Dosis von Dienogest an Tiere in der späten Trächtigkeit und Laktation kann zu einer Beeinträchtigung der Fertilität der Nachkommen führen.
Ethinylestradiol stellt die in den meisten KOK enthaltene östrogene Komponente dar. Bei hohen Dosen wurde eine Embryotoxizität nachgewiesen, und es wurden schädliche Wirkungen auf die Differenzierung urogenitaler Organe beobachtet.
Auf der Grundlage konventioneller Studien liegen keine präklinischen Toxizitätsdaten vor, die besondere Risiken der Genotoxizität und des kanzerogenen Potenzials nach wiederholter Verabreichung des Präparats aufzeigen, außer den oben beschriebenen im Zusammenhang mit der Anwendung kombinierter oraler Kontrazeptiva.
Es sollte jedoch betont werden, dass Sexualhormone das Wachstum von bestimmten hormonabhängigen Geweben und Tumoren fördern können.
06.0 PHARMAZEUTISCHE INFORMATIONEN
06.1 Hilfsstoffe
Kern des Tablets
Lactose-Monohydrat
Magnesiumstearat
Maisstärke
Povidon 30
Talk
Glasur
Opaglos 2 klar, enthält:
Croscarmellose-Natrium
Glucose
Maltodextrin
Natriumcitrat-Dihydrat
Soja Lecithin
06.2 Inkompatibilität
Nicht relevant.
06.3 Gültigkeitsdauer
3 Jahre.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks
PVC / PVDC / Aluminium Blisterpackungen, Packungsgrößen: 21 und 3x21 und 6x21 und 13 X21 Filmtabletten.
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
06.6 Gebrauchs- und Handhabungshinweise
Keine besonderen Hinweise zur Entsorgung.
07.0 INHABER DER MARKETING-ERLAUBNIS
EFFIK ITALIA SpA
Via Lincoln 7 / A
20092 Cinisello Balsamo, Mailand
08.0 NUMMER DER MARKETING-ERLAUBNIS
042101016 - 2 mg / 0,03 mg Filmtabletten "1 x 21 Tabletten im PVC / PVDC / AL Blister
042101028- 2 mg / 0,03 mg Filmtabletten "3 x 21 Tabletten in PVC / PVDC / AL Blisterpackungen
042101030 - 2 mg / 0,03 mg Filmtabletten "6 x 21 Tabletten in PVC / PVDC / AL-Blisterpackungen
042101042- 2 mg / 0,03 mg Filmtabletten "13 x 21 Tabletten in PVC / PVDC / AL-Blisterpackungen
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG
Januar 2013