Um verständlich von der "Hämoglobin (Hb), es ist nützlich, sich um die erste zu kümmern Myoglobin (Mb) die dem Hämoglobin sehr ähnlich ist, aber viel einfacher ist Zwischen Hämoglobin und Myoglobin bestehen enge Verwandtschaftsbeziehungen: Beide sind konjugierte Proteine und ihre prothetische Gruppe (nicht-proteinischer Teil) ist die Gruppe Häm.
Myoglobin ist ein kugelförmiges Protein, das aus einer einzelnen Kette von etwa einhundertfünfzig Aminosäuren besteht (es hängt vom Organismus ab) und sein Molekulargewicht beträgt etwa 18 Kd.
Wie erwähnt, ist es mit einer Hämgruppe ausgestattet, die in einen hydrophoben (oder lipophilen) Teil des Proteins eingefügt ist, der aus Falten besteht, die auf die α-Helix-Strukturen der Faserproteine zurückzuführen sind.
Myoglobin besteht hauptsächlich aus acht Segmenten von α-Helices und besteht fast ausschließlich aus unpolaren Resten (Leucin, Valin, Methionin und Phenylalanin), während polare Reste praktisch fehlen (Asparaginsäure, Glutaminsäure, Lysin). und Arginin); die einzigen polaren Reste sind zwei Histidine, die eine grundlegende Rolle bei der Bindung von Sauerstoff an die Hämgruppe spielen.
Die Hämgruppe ist eine Chromophorgruppe (absorbiert im Sichtbaren) und ist die funktionelle Gruppe von Myoglobin.
Siehe auch: glykiertes Hämoglobin - Hämoglobin im Urin
Ein bisschen Chemie

Die Bindung zwischen Protoporphyrin und Eisen ist eine typische Bindung von Koordinationsverbindungen, bei denen es sich um chemische Verbindungen handelt, in denen ein Zentralatom (oder Ion) Bindungen mit anderen chemischen Spezies in einer höheren Zahl als seiner Oxidationszahl (elektrische Ladung) eingeht. Im Fall von Häm sind diese Bindungen reversibel und schwach.
Die Koordinationszahl (Anzahl der Koordinationsbindungen) von Eisen beträgt sechs: Es können sechs Moleküle um das Eisen herum sein, die sich die Bindungselektronen teilen.
Um eine Koordinationsverbindung zu bilden, braucht es zwei Orbitale mit der richtigen Orientierung: eines kann Elektronen "aufnehmen" und das andere kann sie abgeben.
In Häm bildet Eisen vier planare Bindungen mit den vier Stickstoffatomen im Zentrum des Protoporphyrinrings und eine fünfte Bindung mit einem proximalen Histidin-Stickstoff; Eisen hat die sechste freie Koordinationsbindung und kann an Sauerstoff binden.
Wenn Eisen in Form eines freien Ions vorliegt, sind seine Orbitale D sie haben alle die gleiche Energie; im Myoglobin ist das Eisenion an Protoporphyrin und Histidin gebunden: Diese Spezies stören magnetisch die Orbitale D etwas Eisen; das Ausmaß der Störung wird für die verschiedenen Orbitale unterschiedlich sein D abhängig von ihrer räumlichen Orientierung und der der störenden Spezies. Da die Gesamtenergie der Orbitale konstant sein muss, bewirkt die Störung eine energetische Trennung zwischen den verschiedenen Orbitalen: Die von einigen Orbitalen aufgenommene Energie entspricht der von den anderen verlorenen Energie.
Wenn der Abstand zwischen den Orbitalen nicht sehr groß ist, ist eine elektronische Anordnung mit hohem Spin vorzuziehen: Die Bindungselektronen versuchen, sich in möglichst vielen Unterniveaus in parallelen Spins anzuordnen (maximale Multiplizität); wenn andererseits die Störung sehr stark ist und es einen großen Abstand zwischen den Orbitalen gibt, kann es bequemer sein, die Bindungselektronen in den Orbitalen niedrigerer Energie (niedriger Spin) zu paaren.
Wenn Eisen an Sauerstoff bindet, nimmt das Molekül eine niedrige Spin-Anordnung an, während bei Eisen die sechste Koordinationsbindung frei ist, hat das Molekül eine hohe Spin-Anordnung.
Dank dieser Spindifferenz können wir durch eine Spektralanalyse von Myoglobin verstehen, ob Sauerstoff (MbO2) daran gebunden ist oder nicht (Mb).
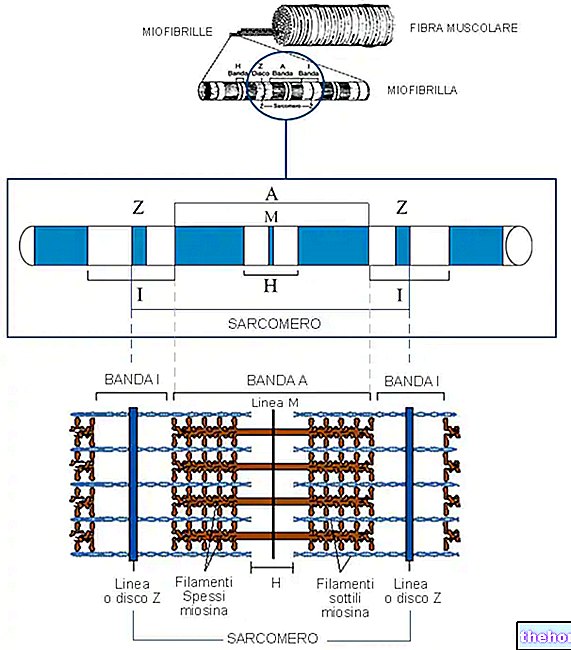
Myoglobin ist ein typisches Muskelprotein (aber es kommt nicht nur in Muskeln vor).
Myoglobin wird aus dem Pottwal, in dem es in großen Mengen vorhanden ist, gewonnen und anschließend gereinigt.
Wale haben eine Atmung wie der Mensch: Da sie eine Lunge haben, müssen sie durch den Atmungsprozess Luft aufnehmen; der Pottwal muss so viel Sauerstoff wie möglich in die Muskeln bringen, die in der Lage sind, Sauerstoff zu akkumulieren, indem er ihn an das in ihnen vorhandene Myoglobin bindet; der Sauerstoff wird dann beim Eintauchen des Wals langsam abgegeben, da sein Stoffwechsel Sauerstoff benötigt: je größer die Menge Sauerstoff, den der Pottwal aufnehmen kann und desto mehr Sauerstoff steht während des Tauchgangs zur Verfügung.
Myoglybin bindet Sauerstoff reversibel und ist in peripheren Geweben zu einem größeren Prozentsatz vorhanden, je mehr das Gewebe daran gewöhnt ist, mit zeitlich entfernten Sauerstoffvorräten zu arbeiten.
<--- Myoglobin ist ein in den Muskeln vorhandenes Protein, dessen Funktion genau die eines Sauerstoff-„Reservoirs“ ist.
Was das Fleisch mehr oder weniger rot macht, ist der Gehalt an Hämoproteinen (es ist das Häm, das das Fleisch rot macht).
Hämoglobin weist viele strukturelle Ähnlichkeiten mit Myoglobin auf und ist in der Lage, molekularen Sauerstoff reversibel zu binden; aber während Myoglobin im Allgemeinen auf Muskeln und peripheres Gewebe beschränkt ist, wird Hämoglobin in Erythrozyten oder roten Blutkörperchen (sie sind Pseudozellen, d. h. keine echten Zellen) gefunden, die 40% des Blutes ausmachen.
Im Gegensatz zu Myoglobin besteht die Aufgabe von Hämoglobin darin, Sauerstoff in die Lunge aufzunehmen, ihn dort an die Zellen abzugeben, wo er benötigt wird, Kohlendioxid aufzunehmen und in die Lunge abzugeben, wo der Kreislauf erneut beginnt.
L"Hämoglobin es ist ein Tetrameter, das heißt, es besteht aus vier Polypeptidketten mit jeweils einer Hämgruppe und zwei mal zwei identisch (beim Menschen gibt es zwei Alpha-Ketten und zwei Beta-Ketten).
Die Hauptfunktion des Hämoglobins ist der Transport von Sauerstoff, eine weitere Funktion des Blutes, an der Hämoglobin beteiligt ist, ist der Transport von Stoffen zu den Geweben.
Auf dem Weg von der Lunge (sauerstoffreich) zu den Geweben transportiert Hämoglobin Sauerstoff (gleichzeitig gelangen die anderen Stoffe in das Gewebe), während es auf dem umgekehrten Weg die vom Gewebe gesammelten Abfälle, insbesondere den Kohlenstoff, mitnimmt im Stoffwechsel produziertes Dioxid.
In der Entwicklung eines Menschen gibt es Gene, die nur für einen bestimmten Zeitraum exprimiert werden; Aus diesem Grund gibt es verschiedene Hämoglobine: fötal, embryonal, des erwachsenen Mannes.
Die Ketten, aus denen diese verschiedenen Hämoglobine bestehen, haben unterschiedliche Strukturen, aber mit einigen Ähnlichkeiten ist die Funktion, die sie erfüllen, mehr oder weniger gleich.
Eine Erklärung für das Vorhandensein mehrerer unterschiedlicher Ketten ist folgende: Im Laufe der Evolution der Organismen hat sich sogar das Hämoglobin entwickelt, das sich auf den Transport von Sauerstoff aus sauerstoffreichen Gebieten in mangelhafte Gebiete spezialisiert hat der Evolutionskette l" Hämoglobin transportierte Sauerstoff in kleinen Organismen; im Laufe der Evolution erreichten die Organismen größere Dimensionen, daher wurde das Hämoglobin so modifiziert, dass es Sauerstoff in Gebiete transportieren kann, die weiter weg von der Stelle, an der es reich war; Dafür wurden ihnen im Laufe des Evolutionsprozesses neue Strukturen der Ketten, aus denen Hämoglobin besteht, codiert.
Myoglobin bindet schon bei geringen Drücken Sauerstoff, in den peripheren Geweben herrscht ein Druck (PO2) von etwa 30 mmHg: Myoglobin setzt bei diesem Druck keinen Sauerstoff frei, wäre also als Sauerstoffträger unwirksam, das Hämoglobin hingegen , es hat ein elastischeres Verhalten: Es bindet Sauerstoff bei hohem Druck und gibt ihn bei Druckabfall wieder ab.
Wenn ein Protein funktionell aktiv ist, kann es seine Form ein wenig ändern; zum Beispiel hat mit Sauerstoff angereichertes Myoglobin eine andere Form als nicht mit Sauerstoff angereichertes Myoglobin und diese Mutation beeinflusst seine Nachbarn nicht.
Anders verhält es sich bei assoziierten Proteinen wie Hämoglobin: Wenn eine Kette mit Sauerstoff angereichert wird, ändert sich ihre Form, aber diese Modifikation ist dreidimensional, so dass auch die anderen Ketten des Tetrameters betroffen sind miteinander Oxygenate nimmt ab, da die Ketten in der Nähe ihrerseits Oxygenate anreichern. Das gleiche gilt für die Desoxygenierung.
Die Quartärstruktur von Desoxyhämoglobin wird als T-Form (angespannt) bezeichnet, während die von Oxyhämoglobin als R-Form (freigesetzt) bezeichnet wird; im angespannten Zustand gibt es eine Reihe ziemlich starker elektrostatischer Wechselwirkungen zwischen sauren Aminosäuren und basischen Aminosäuren, die zu einer starren Struktur von Desoxyhämoglobin führen (deshalb die "angespannte Form"), während wenn Sauerstoff verbunden ist, die Einheit dieser Wechselwirkungen nimmt ab (daher die "freigegebene Form"). Außerdem wird in Abwesenheit von Sauerstoff die Ladung des Histidins (siehe Struktur) durch die entgegengesetzte Ladung der Asparaginsäure stabilisiert, während in Gegenwart von Sauerstoff das Protein dazu neigt, ein Proton zu verlieren; All dies beinhaltet, dass sauerstoffreiches Hämoglobin eine stärkere Säure ist als sauerstoffarmes Hämoglobin: Bohr-Effekt.
Je nach pH-Wert bindet die Hämgruppe mehr oder weniger leicht an Sauerstoff: Hämoglobin gibt im sauren Milieu leichter Sauerstoff ab (die gespannte Form ist stabil), während im basischen Milieu die Bindung an Sauerstoff härter ist.

Jedes Hämoglobin setzt 0,7 Protonen pro eintretendem Mol Sauerstoff (O2) frei.
Der Bohr-Effekt ermöglicht es Hämoglobin, seine Fähigkeit, Sauerstoff zu transportieren, zu verbessern.
Das Hämoglobin, das von der Lunge in die Gewebe gelangt, muss sich in Abhängigkeit von Druck, pH-Wert und Temperatur ausgleichen.
Sehen wir uns den Temperatureffekt an.
Die Temperatur in den Lungenbläschen ist etwa 1-1,5 °C niedriger als die Außentemperatur, während die Temperatur in den Muskeln etwa 36,5-37 °C beträgt; mit steigender Temperatur sinkt der Sättigungsfaktor (bei gleichem Druck): Dies geschieht, weil die kinetische Energie zunimmt und die Dissoziation begünstigt wird.

Es gibt andere Faktoren, die die Fähigkeit von Hämoglobin, an Sauerstoff zu binden, beeinflussen können, einer davon ist die Konzentration von 2,3-Bisphosphoglycerat.
2,3-Bisphosphoglycerat ist ein Stoffwechselprodukt, das in Erythrozyten in einer Konzentration von 4-5 mM vorhanden ist (in keinem anderen Teil des Organismus ist es in so hoher Konzentration vorhanden).
Bei physiologischem pH-Wert ist 2,3-Bisphosphoglycerat deprotoniert und weist fünf negative Ladungen auf; es ist zwischen den beiden Betaketten des Hämoglobins eingeklemmt, weil diese Ketten eine hohe Konzentration an positiven Ladungen aufweisen. Die elektrostatischen Wechselwirkungen zwischen den Betaketten und dem 2,3-Bisphosphoglycerat verleihen dem System eine gewisse Steifigkeit: Es entsteht eine gespannte Struktur mit geringer Affinität zu Sauerstoff, bei der Oxygenierung wird dann das 2,3-Bisphosphoglycerat ausgestoßen.
In Erythrozyten ist c" ein spezieller Apparat, der 1,3-Bisphosphoglycerat (durch Stoffwechsel produziert) in 2,3-Bisphosphoglycerat umwandelt, so dass es eine Konzentration von 4-5 mM erreicht und somit das Hämoglobin in der Lage ist, den "Sauerstoff im Gewebe auszutauschen.
Das im Gewebe ankommende Hämoglobin befindet sich im freigesetzten Zustand (an Sauerstoff gebunden), wird jedoch in der Nähe des Gewebes carboxyliert und geht in den angespannten Zustand über: Das Protein in diesem Zustand neigt weniger zur Bindung an Sauerstoff, bzgl in den freigesetzten Zustand, daher gibt Hämoglobin Sauerstoff an das Gewebe ab; außerdem entstehen durch reaktion zwischen wasser und kohlendioxid H + ionen, also weiterer sauerstoff durch den bohr-effekt.
Kohlendioxid diffundiert in die Erythrozyten, die die Plasmamembran passieren; Da Erythrozyten etwa 40% des Blutes ausmachen, sollten wir erwarten, dass nur 40% des Kohlendioxids, das aus den Geweben diffundiert, in sie gelangt, tatsächlich gelangen 90% des Kohlendioxids in die Erythrozyten, weil sie ein Enzym enthalten, das Kohlendioxid umwandelt in Kohlensäure führt dies dazu, dass die stationäre Kohlendioxidkonzentration in den Erythrozyten gering und damit die Eintrittsrate hoch ist.

Ein weiteres Phänomen, das auftritt, wenn ein Erythrozyten ein Gewebe erreicht, ist folgendes: Durch einen Gradienten verlässt das "HCO3- (Derivat von Kohlendioxid) den" Erythrozyten und, um die Ausgabe einer negativen Ladung auszugleichen, haben wir den " Eintritt von Chloriden, die bestimmt eine Erhöhung des osmotischen Drucks: zum Ausgleich dieser Schwankung gibt es auch den Wassereintritt, der zu einer Schwellung der Erythrozyten führt (HAMBURGER-Effekt) Das gegenteilige Phänomen tritt auf, wenn ein Erythrozyten die Lungenbläschen erreicht: eine Deflation der Erythrozyten (HALDANE-Effekt) Daher sind die venösen (zu den Lungen gerichteten) Erythrozyten runder als die arteriellen.


.jpg)