Wirkstoffe: Teicoplanin
TARGOSID 200 mg Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen
TARGOSID 400 mg Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen
Indikationen Warum wird Targosid angewendet? Wofür ist das?
Targosid ist ein Antibiotikum, das den Wirkstoff "Teicoplanin" enthält. Es wirkt, indem es die Bakterien abtötet, die für Infektionen im Körper verantwortlich sind.
Targosid wird bei Erwachsenen und Kindern (einschließlich Säuglingen) zur Behandlung von bakteriellen Infektionen angewendet von:
- Haut und darunterliegendes Gewebe (manchmal auch als "Weichgewebe" bezeichnet)
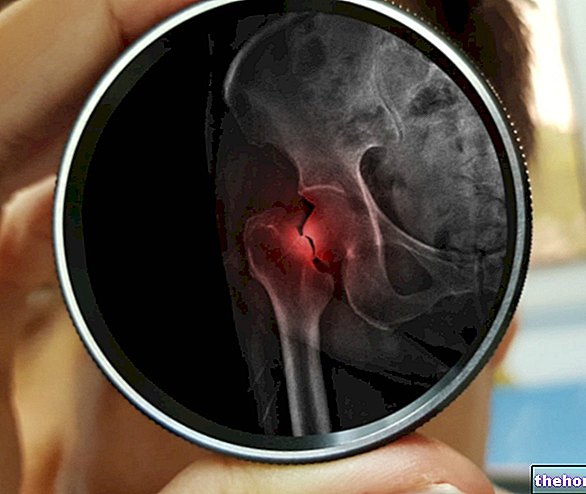
- Knochen und Gelenke
- Lunge
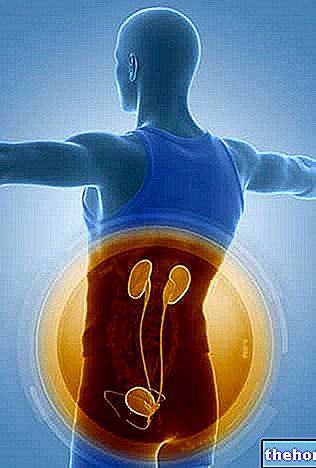
- Harntrakt
- Herz (Endokarditis)
- Bauchbereich (Peritonitis)
- Blut, wenn es durch eine der oben aufgeführten Bedingungen verursacht wird.
Targosid kann zur Behandlung bestimmter Infektionen, die durch Clostridium-difficile-Bakterien im Darm verursacht werden, angewendet werden, wobei die Lösung oral eingenommen wird.
Kontraindikationen Wenn Targosid nicht angewendet werden sollte
Verwenden Sie Targosid nicht, wenn:
- wenn Sie allergisch gegen Teicoplanin oder einen der sonstigen Bestandteile dieses Arzneimittels sind
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Targosid® beachten?
Bitte sprechen Sie mit Ihrem Arzt, Apotheker oder dem medizinischen Fachpersonal, bevor Sie Targocid erhalten, wenn:
- Sie allergisch gegen ein Antibiotikum namens "Vancomycin" sind
- eine Rötung des Oberkörpers (Red Neck Syndrom) haben
- eine Abnahme der Thrombozytenzahl haben (Thrombozytopenie)
- Nierenprobleme haben
- Sie andere Arzneimittel einnehmen, die Hör- und/oder Nierenprobleme verursachen können. Möglicherweise müssen Sie regelmäßig untersucht werden, ob Ihr Blut, Ihre Nieren und Ihre Leber richtig funktionieren (siehe „Einnahme von Targosid zusammen mit anderen Arzneimitteln“).
Wenn einer der oben genannten Punkte auf Sie zutrifft (oder wenn Sie sich nicht sicher sind), sprechen Sie mit Ihrem Arzt, Apotheker oder dem medizinischen Fachpersonal, bevor Sie Targosid erhalten.
Prüfungen
Möglicherweise müssen Sie während der Behandlung Tests zur Überprüfung Ihrer Nieren und/oder Ihres Gehörs durchführen lassen.Dies ist wahrscheinlicher, wenn:
- die Behandlung wird lange dauern
- Nierenprobleme haben
- Sie andere Arzneimittel einnehmen, die das Nervensystem, die Nieren oder das Gehör beeinträchtigen können oder beabsichtigen, diese einzunehmen.
Bei Patienten, die Targosid über einen längeren Zeitraum erhalten, können Bakterien, die durch das Antibiotikum nicht beeinflusst werden, stärker als normal wachsen – der Arzt wird dies überprüfen.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Targosid® beeinflussen?
Informieren Sie Ihren Arzt, Apotheker oder das medizinische Fachpersonal, wenn Sie andere Arzneimittel einnehmen, kürzlich andere Arzneimittel eingenommen haben oder beabsichtigen andere Arzneimittel einzunehmen, da Targosid die Wirkung einiger anderer Arzneimittel beeinflussen kann. Auch einige Arzneimittel können die Wirkungsweise von Targosid beeinflussen.
Informieren Sie Ihren Arzt, Apotheker oder das medizinische Fachpersonal insbesondere, wenn Sie eines der folgenden Arzneimittel einnehmen:
- Aminoglykoside, die nicht mit Targosid in derselben Injektion gemischt werden dürfen. Sie können auch Hörprobleme und/oder Nierenprobleme verursachen.
- Amphotericin B – ein Arzneimittel zur Behandlung von Pilzinfektionen, die Hörprobleme und/oder Nierenprobleme verursachen können
- Ciclosporin – ein Arzneimittel, das das Immunsystem beeinflusst und zu Hörproblemen und/oder Nierenproblemen führen kann
- Cisplatin – ein Arzneimittel zur Behandlung von bösartigen Tumoren, die Hörprobleme und/oder Nierenprobleme verursachen können
- Diuretika (wie Furosemid), die Hörprobleme und/oder Nierenprobleme verursachen können
Wenn einer der oben genannten Punkte auf Sie zutrifft (oder wenn Sie sich nicht sicher sind), sprechen Sie mit Ihrem Arzt oder Apotheker oder dem medizinischen Fachpersonal, bevor Sie Targosid erhalten.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft, Stillzeit und Fruchtbarkeit
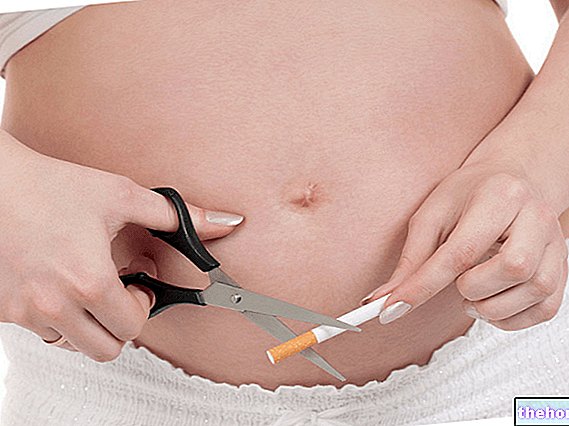
Wenn Sie schwanger sind, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Anwendung dieses Arzneimittels Ihren Arzt, Apotheker oder das medizinische Fachpersonal um Rat.
Sie werden entscheiden, ob Sie dieses Arzneimittel während der Schwangerschaft erhalten. Es kann ein potenzielles Risiko für Innenohr- und Nierenprobleme bestehen.
Informieren Sie Ihren Arzt, wenn Sie stillen, bevor Sie dieses Arzneimittel erhalten. Sie entscheiden, ob Sie während der Behandlung mit Targosid weiter stillen können oder nicht. Reproduktionsstudien an Tieren haben keine Hinweise auf Fruchtbarkeitsprobleme ergeben.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Während der Behandlung mit Targosid können Sie Kopfschmerzen oder Schwindel haben. Fahren Sie in diesem Fall kein Fahrzeug und bedienen Sie keine Maschinen.
Targosid enthält Natrium
Dieses Arzneimittel enthält weniger als 1 mmol Natrium (23 mg) pro Durchstechflasche, d. h. es ist praktisch natriumfrei.
Dosis, Methode und Zeitpunkt der Anwendung Wie ist Targosid anzuwenden: Dosierung
Die empfohlene Dosis beträgt
Erwachsene und Kinder (ab 12 Jahren) ohne Nierenprobleme
Infektionen der Haut und des Unterhautzellgewebes, der Lunge und der Harnwege
- Anfangsdosis (für die ersten 3 Dosen): 400 mg (entsprechend 6 mg pro kg Körpergewicht) alle 12 Stunden durch Injektion in eine Vene oder einen Muskel
- Erhaltungsdosis: 400 mg (entsprechend 6 mg pro kg Körpergewicht) einmal täglich als Injektion in eine Vene oder einen Muskel verabreicht
Infektionen der Knochen und Gelenke und des Herzens
- Anfangsdosis (für die ersten 3-5 Dosen): 800 mg (entsprechend 12 mg pro kg Körpergewicht) alle 12 Stunden durch Injektion in eine Vene oder einen Muskel
- Erhaltungsdosis: 800 mg (entsprechend 12 mg pro kg Körpergewicht) einmal täglich als Injektion in eine Vene oder einen Muskel verabreicht
Zur Behandlung von Infektionen durch Clostridium-difficile-Bakterien
Die empfohlene Dosis beträgt 100-200 mg zweimal täglich für 7 bis 14 Tage
Erwachsene und ältere Patienten mit Nierenproblemen
Wenn Sie Nierenprobleme haben, wird Ihre Dosis normalerweise nach dem vierten Behandlungstag verringert:
- Bei Personen mit leichten und mittelschweren Nierenproblemen wird die Erhaltungsdosis alle 2 Tage oder täglich die Hälfte der Erhaltungsdosis verabreicht.
- Bei Patienten mit schweren Nierenproblemen oder Hämodialysepatienten: Die Erhaltungsdosis wird alle 3 Tage oder täglich ein Drittel der Erhaltungsdosis verabreicht.
Peritonitis bei Peritonealdialysepatienten
Die Anfangsdosis beträgt 6 mg pro kg Körpergewicht, verabreicht als Einzelinjektion in eine Vene, gefolgt von:
- Woche eins: 20 mg/L in jedem Dialysebeutel
- Woche zwei: 20 mg/L in abwechselnden Beuteln
- Woche drei: 20 mg/L in der Reisetasche.
Kleinkinder (ab Geburt bis 2 Monate)
- Anfangsdosis (am ersten Tag): 16 mg pro kg Körpergewicht, als Infusion durch Tropfen in eine Vene
- Erhaltungsdosis: 8 mg pro kg Körpergewicht, einmal täglich als Infusion in eine Vene verabreicht.
Kinder (2 Monate bis 12 Jahre)
- Anfangsdosis (für die ersten drei Dosen): 10 mg pro kg Körpergewicht alle 12 Stunden als Injektion in eine Vene
- Erhaltungsdosis: 6 - 10 mg pro kg Körpergewicht einmal täglich als Injektion in eine Vene
Wie Targosid verabreicht wird
Dieses Arzneimittel wird normalerweise von einem Arzt oder einer Krankenschwester verabreicht
- es wird durch Injektion in eine Vene (intravenös) oder in einen Muskel (intramuskulär) verabreicht.
- es kann auch als Infusion mit Tropfen in eine Vene verabreicht werden.
Säuglinge von der Geburt bis zum Alter von 2 Monaten sollten nur als Infusion verabreicht werden.
Zur Behandlung einiger Infektionen kann die Lösung oral eingenommen werden (orale Anwendung).
Überdosierung Was ist zu tun, wenn Sie zu viel Targosid eingenommen haben?
Wenn Sie eine größere Menge von Targosid erhalten haben, als Sie sollten
Es ist unwahrscheinlich, dass Ihr Arzt oder das medizinische Fachpersonal Ihnen zu viel des Arzneimittels verschreiben wird.
Wenn Sie die Einnahme von Targosid® vergessen haben
Ihr Arzt oder das medizinische Fachpersonal werden Anweisungen haben, wann Targosid verabreicht werden soll.Es ist unwahrscheinlich, dass sie Ihnen das Arzneimittel nicht wie verordnet verabreichen.Wenn Sie jedoch besorgt sind, informieren Sie Ihren Arzt oder das medizinische Fachpersonal.
Wenn Sie die Einnahme von Targosid® abbrechen
Brechen Sie die Einnahme dieses Arzneimittels nicht ab, ohne vorher mit Ihrem Arzt, Apotheker oder dem medizinischen Fachpersonal gesprochen zu haben.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal.
Nebenwirkungen Was sind die Nebenwirkungen von Targosid
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Schwere Nebenwirkungen
Brechen Sie die Behandlung ab und informieren Sie sofort Ihren Arzt oder das medizinische Fachpersonal, wenn Sie eine der folgenden schwerwiegenden Nebenwirkungen bemerken – Sie benötigen möglicherweise dringend ärztliche Behandlung:
Gelegentlich (kann bis zu 1 von 100 Patienten betreffen)
- plötzliche allergische Reaktion, die lebensbedrohlich sein kann - die Anzeichen können sein: Atembeschwerden oder pfeifende Atmung, Schwitzen, Hautausschlag, Juckreiz, Fieber, Schüttelfrost
Selten (kann bis zu 1 von 1.000 Patienten betreffen)
- Flush im Oberkörper Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
- Läsionen der Haut, des Mundes, der Augen oder der Genitalien – dies können Anzeichen einer Erkrankung sein, die als „toxische epidermale Nekrolyse“ oder „Stevens-Johnson-Syndrom“ bezeichnet wird.
Informieren Sie sofort Ihren Arzt oder das medizinische Fachpersonal, wenn Sie eine der oben aufgeführten Nebenwirkungen bemerken.
Informieren Sie sofort Ihren Arzt oder das medizinische Fachpersonal, wenn Sie eine der folgenden schwerwiegenden Nebenwirkungen bemerken – Sie benötigen möglicherweise dringend ärztliche Behandlung:
Gelegentlich (kann bis zu 1 von 100 Patienten betreffen)
- Schwellung und Gerinnung in einer Vene
- Schwierigkeiten beim Atmen oder Keuchen (Bronchospasmus)
- erhöhte Anzahl von Infektionen – dies können Anzeichen für eine Abnahme der Anzahl der Blutkörperchen sein
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
- Mangel an weißen Blutkörperchen – Anzeichen können sein: Fieber, starke Schüttelfrost, Halsschmerzen oder Geschwüre im Mund (Agranulozytose)
- Nierenprobleme oder Veränderungen der Nierenfunktion - in Tests nachgewiesen
- Anfälle
Informieren Sie sofort Ihren Arzt oder das medizinische Fachpersonal, wenn Sie eine der oben aufgeführten Nebenwirkungen bemerken.
Andere Nebenwirkungen
Informieren Sie Ihren Arzt, Apotheker oder das medizinische Fachpersonal, wenn Sie eines der folgenden Symptome bemerken:
Häufig (kann bis zu 1 von 10 Patienten betreffen)
- Hautausschlag, Erythem, Juckreiz
- Schmerzen
- Fieber
Gelegentlich (kann bis zu 1 von 100 Patienten betreffen)
- Abnahme der Thrombozytenzahl
- erhöhte Leberenzymwerte im Blut
- erhöhte Kreatininwerte im Blut (zur Kontrolle der Nieren)
- Hörverlust, Klingeln in Ihren Ohren oder das Gefühl, dass Sie oder Dinge um Sie herum sich bewegen
- Übelkeit oder Erbrechen (Erbrechen), Durchfall
- Schwindel oder Kopfschmerzen
Selten (kann bis zu 1 von 1.000 Patienten betreffen)
- Infektion (Abszess)
Nicht bekannt (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
- Probleme an der Injektionsstelle - wie Rötung der Haut, Schmerzen oder Schwellungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt, Apotheker oder das medizinische Fachpersonal, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind.
Ablauf und Aufbewahrung
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Verwenden Sie dieses Arzneimittel nicht nach dem auf dem Karton und dem Etikett der Durchstechflasche nach EXP / EXP angegebenen Verfallsdatum Das Verfallsdatum bezieht sich auf den letzten Tag dieses Monats.
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Informationen zur Lagerung und Verwendungsdauer von Targosid, nachdem es rekonstituiert und gebrauchsfertig ist, sind in den „Praktischen Informationen für medizinisches Fachpersonal zur Zubereitung und Handhabung von Targosid“ beschrieben.
Was Targosid enthält
- Der Wirkstoff ist Teicoplanin. Jede Durchstechflasche enthält 200 mg oder 400 mg Teicoplanin.
- Die sonstigen Bestandteile sind Natriumchlorid und Natriumhydroxid in Pulverform und Wasser für Injektionszwecke im Lösungsmittel.
Beschreibung wie Targosid aussieht und Inhalt der Packung
Targosid ist ein Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder einer Lösung zum Einnehmen. Das Pulver ist eine schwammige, homogene Masse von Elfenbeinfarbe. Das Lösungsmittel ist eine klare, farblose Flüssigkeit.
Das Pulver ist verpackt:
- in farblosen Durchstechflaschen aus Typ-I-Glas mit einem Nutzvolumen von 10 ml für 200 mg, verschlossen mit einem Brombutyl-Gummistopfen, einer gelben Aluminiumkappe und einer Abreißlasche aus Kunststoff.
- in farblosen Durchstechflaschen aus Typ-I-Glas mit einem Nutzvolumen von 22 ml für 400 mg, verschlossen mit einem Brombutyl-Gummistopfen, einer grünen Aluminiumkappe und einer Abreißlasche aus Kunststoff.
Das Lösungsmittel ist in einem farblosen Glasfläschchen vom Typ I verpackt.
Verpackung:
- 1 Durchstechflasche Pulver mit 1 Durchstechflasche Lösungsmittel
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht
Die folgenden Informationen sind nur für Ärzte oder medizinisches Fachpersonal bestimmt:
Praktische Informationen für medizinisches Fachpersonal zur Zubereitung und Handhabung von Targosid.
Dieses Arzneimittel ist nur zur einmaligen Anwendung bestimmt.
Art der Verabreichung
Die rekonstituierte Lösung kann direkt injiziert oder alternativ weiter verdünnt werden.
Die Injektion kann als 3-5-minütiger Bolus oder als 30-minütige Infusion verabreicht werden.
Säuglinge von der Geburt bis zum Alter von 2 Monaten sollten nur als Infusion verabreicht werden.
Die rekonstituierte Lösung kann auch oral verabreicht werden (orale Anwendung).
Zubereitung der rekonstituierten Lösung
- Injizieren Sie langsam den gesamten Inhalt der Durchstechflasche mit dem Lösungsmittel in die Durchstechflasche mit dem Pulver
- Schwenken Sie die Durchstechflasche vorsichtig zwischen Ihren Händen, bis sich das Pulver vollständig aufgelöst hat. Wenn die Lösung schaumig wird, lassen Sie sie etwa 15 Minuten einwirken.
Die rekonstituierten Lösungen enthalten 200 mg Teicoplanin in 3,0 ml und 400 mg in 3,0 ml.
Es sollten nur klare und gelbliche Lösungen verwendet werden.
Die endgültige Lösung ist isotonisch mit Plasma und hat einen pH-Wert von 7,2 bis 7,8.
Zubereitung der verdünnten Lösung vor der Infusion
Targosid kann in folgenden Infusionslösungen verabreicht werden:
- Natriumchloridlösung 9 mg / ml (0,9%)
- Ringer-Lösung
- Ringer-Laktatlösung
- 5% Dextroselösung
- 10% Dextroselösung
- Lösung mit 0,18 % Natriumchlorid und 4 % Glucose
- Lösung mit 0,45% Natriumchlorid und 5% Glucose
- Peritonealdialyselösung mit 1,36% oder 3,86% Glucoselösung.
Haltbarkeit der rekonstituierten Lösung
Die chemisch-physikalische Stabilität der gemäß den Empfehlungen hergestellten rekonstituierten Lösung wurde für 24 Stunden bei einer Temperatur zwischen 2 und 8 ° C nachgewiesen.
Aus mikrobiologischer Sicht sollte das Produkt sofort verwendet werden. Geschieht dies nicht, ist der Benutzer für die Lagerzeit und die Bedingungen des Produkts verantwortlich, die normalerweise 24 Stunden bei einer Temperatur zwischen 2 und 8 ° C nicht überschreiten sollten, es sei denn, die Rekonstitution wird unter kontrollierten und validierten Bedingungen durchgeführt.
Haltbarkeit des verdünnten Arzneimittels
Die chemisch-physikalische Stabilität der gemäß den Empfehlungen hergestellten rekonstituierten Lösung wurde für 24 Stunden bei einer Temperatur zwischen 2 und 8 ° C nachgewiesen. Aus mikrobiologischer Sicht sollte das Produkt sofort verwendet werden. Wenn dies nicht der Fall ist, ist der Benutzer für die Lagerdauer und die Bedingungen des Produkts verantwortlich und sollte normalerweise 24 Stunden bei einer Temperatur zwischen 2 und 8 ° C nicht überschreiten, es sei denn, die Rekonstitution / Verdünnung wird unter kontrollierten Bedingungen durchgeführt durch Asepsis validiert.
Entsorgung
Nicht verwendete Arzneimittel und Abfälle aus diesem Arzneimittel müssen gemäß den örtlichen Vorschriften entsorgt werden.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS
TARGOSID-PULVER UND LÖSUNGSMITTEL FÜR INJIZIERBARE LÖSUNG / INFUSION ODER ORALE LÖSUNG
▼ Arzneimittel, das einer zusätzlichen Überwachung unterliegt. Dies ermöglicht die schnelle Identifizierung neuer Sicherheitsinformationen. Angehörige von Gesundheitsberufen sind aufgefordert, jeden Verdachtsfall einer Nebenwirkung zu melden. Siehe Abschnitt 4.8 für Informationen zur Meldung von Nebenwirkungen.
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG
Jede Durchstechflasche enthält 200 mg Teicoplanin, entsprechend mindestens 200.000 IE.
Nach der Rekonstitution enthält die Lösung 200 mg Teicoplanin in 3,0 ml.
Jede Durchstechflasche enthält 400 mg Teicoplanin, entsprechend mindestens 400.000 IE.
Nach der Rekonstitution enthält die Lösung 400 mg Teicoplanin in 3,0 ml.
Die vollständige Auflistung der sonstigen Bestandteile finden Sie in Abschnitt 6.1.
03.0 DARREICHUNGSFORM
Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen.
Pulver zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen: elfenbeinfarbene schwammartige homogene Masse.
Lösungsmittel: klare, farblose Flüssigkeit.
04.0 KLINISCHE INFORMATIONEN
04.1 Anwendungsgebiete
Targosid ist angezeigt bei Erwachsenen und Kindern ab der Geburt zur parenteralen Behandlung der folgenden Infektionen (siehe Abschnitte 4.2, 4.4 und 5.1):
• komplizierte Haut- und Weichteilinfektionen,
• Knochen- und Gelenkinfektionen,
• im Krankenhaus erworbene Lungenentzündung,
• ambulant erworbene Lungenentzündung,
• komplizierte Harnwegsinfektionen,
• infektiösen Endokarditis,
• Peritonitis in Verbindung mit kontinuierlicher ambulanter Peritonealdialyse (CAPD),
• Bakteriämie, die in Verbindung mit einer der oben aufgeführten Indikationen auftritt.
Targosid ist auch als alternative orale Therapie bei der Behandlung von Durchfall und Kolitis im Zusammenhang mit Infektionen indiziert Clostridium difficile.
Gegebenenfalls kann Teicoplanin in Kombination mit anderen antibakteriellen Arzneimitteln verabreicht werden.
Offizielle Richtlinien zur angemessenen Anwendung antibakterieller Arzneimittel sollten berücksichtigt werden.
04.2 Dosierung und Art der Anwendung
Dosierung
Dosis und Dauer der Behandlung sollten individuell an Art und Schwere der Infektion, klinisches Ansprechen des Patienten und patientenbezogene Parameter wie Alter und Nierenfunktion angepasst werden.
Messung von Serumkonzentrationen
Um die Behandlung zu optimieren, sollten die Teicoplanin-Serumkonzentrationen im Steady-State nach Abschluss des Belastungsschemas überwacht werden, um sicherzustellen, dass die erforderlichen Mindestkonzentrationen erreicht wurden:
• Bei den meisten Gram-positiven Infektionen sind Teicoplanin-Talspiegel von mindestens 10 mg/l, gemessen mit High Liquid Performance Chromatography (HPLC), oder 15 mg/l, gemessen mit der Fluoreszenz-Polarisations-Immunoassay-(FPIA)-Methode.
• Bei Endokarditis und anderen schweren Infektionen Teicoplanin-Talspiegel von 15-30 mg/l bei Messung mit HPLC oder 30-40 mg/l bei Messung mit FPIA-Methode.
Während der Erhaltungstherapie kann mindestens einmal wöchentlich eine Überwachung der erforderlichen Talkonzentrationen erfolgen, um sicherzustellen, dass diese Konzentrationen stabil sind.
Erwachsene und ältere Menschen mit normaler Nierenfunktion
1 Gemessen mit FPIA
Dauer der Behandlung
Die Behandlungsdauer sollte sich nach dem klinischen Ansprechen richten. Bei einer infektiösen Endokarditis werden in der Regel mindestens 21 Tage als angemessen erachtet, die Behandlung sollte 4 Monate nicht überschreiten.
Kombinationsbehandlung
Teicoplanin hat ein begrenztes antibakterielles Wirkungsspektrum (grampositiv). Es ist nicht als Einzelwirkstoff zur Behandlung bestimmter Infektionsarten geeignet, es sei denn, der Erreger ist bereits bekannt und von bekannter Anfälligkeit oder es besteht ein hoher Verdacht, dass der wahrscheinlichste Erreger (die wahrscheinlichsten Erreger) für eine Behandlung (nicht) empfänglich sind mit Teicoplanin.
Durchfall und Kolitis im Zusammenhang mit einer Clostridium-difficile-Infektion
Die empfohlene Dosis beträgt 100-200 mg zweimal täglich oral über 7 bis 14 Tage.
Ältere Patienten
Eine Dosisanpassung ist nicht erforderlich, es sei denn, es liegt eine Niereninsuffizienz vor (siehe unten).
Erwachsene und ältere Patienten mit Niereninsuffizienz
Bis zum vierten Behandlungstag ist keine Dosisanpassung erforderlich, ab dem die Dosis angepasst werden muss, um die Talspiegelkonzentrationen von mindestens 10 mg / L aufrechtzuerhalten.
Nach dem vierten Behandlungstag:
• bei leichter und mittelschwerer Niereninsuffizienz (Kreatinin-Clearance zwischen 30 und 80 ml/min): Die Erhaltungsdosis sollte halbiert werden, indem die Dosis jeden zweiten Tag oder einmal täglich die halbe Dosis verabreicht wird.
• bei schwerer Niereninsuffizienz (Kreatinin-Clearance weniger als 30 ml/min) und bei Patienten, die sich einer Hämodialyse unterziehen: Die Dosis sollte ein Drittel der normalen Dosis betragen, die alle 3 Tage verabreicht wird, oder ein Drittel der Dosis einmal täglich.
Teicoplanin wird nicht durch Hämodialyse entfernt.
Patienten mit kontinuierlicher ambulanter Peritonealdialyse (CAPD)
Nach einer einmaligen intravenösen Aufsättigungsdosis von 6 mg/kg Körpergewicht werden in der ersten Woche 20 mg/L in allen Dialyselösungsbeuteln, in der zweiten Woche 20 mg/L in abwechselnden Beuteln und danach 20 mg/L verabreicht die Nachttasche während der dritten Woche.
Kinder und Jugendliche
Die empfohlenen Dosierungen sind bei Erwachsenen und Kindern über 12 Jahren gleich.
Babys und Kinder von der Geburt bis 2 Monate :
Ladedosis
Eine Einzeldosis von 16 mg / kg Körpergewicht, verabreicht durch intravenöse Infusion am ersten Tag
Erhaltungsdosis
Eine Einzeldosis von 8 mg / kg Körpergewicht, verabreicht durch intravenöse Infusion einmal täglich.
Kinder (2 Monate bis 12 Jahre) :
Ladedosis
Eine Einzeldosis von 10 mg / kg Körpergewicht, intravenös alle 12 Stunden verabreicht, 3-mal wiederholt
Erhaltungsdosis
Einmal täglich eine Einzeldosis von 6-10 mg/kg Körpergewicht intravenös verabreicht
Art der Verabreichung
Teicoplanin muss intravenös oder intramuskulär verabreicht werden.
Die intravenöse Injektion kann entweder als 3-5-minütiger Bolus oder als 30-minütige Infusion verabreicht werden.
Bei Neugeborenen sollte nur eine Infusion verwendet werden.
Anweisungen zur Rekonstitution und Verdünnung des Arzneimittels vor der Anwendung siehe Abschnitt 6.6.
04.3 Kontraindikationen
Überempfindlichkeit gegen Teicoplanin oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung
Überempfindlichkeitsreaktionen
Unter Teicoplanin wurden schwerwiegende, lebensbedrohliche und manchmal tödliche Überempfindlichkeitsreaktionen berichtet (z. B. anaphylaktischer Schock). Wenn eine allergische Reaktion auf Teicoplanin auftritt, sollte die Behandlung sofort abgebrochen und geeignete Notfallmaßnahmen ergriffen werden.
Teicoplanin sollte bei Patienten mit bekannter Überempfindlichkeit gegen Vancomycin mit Vorsicht angewendet werden, da Kreuzüberempfindlichkeitsreaktionen, einschließlich tödlichem anaphylaktischem Schock, auftreten können.
Ein „Red-Man-Syndrom“ in der Vorgeschichte mit Vancomycin ist jedoch keine Kontraindikation für die Anwendung von Teicoplanin.
Infusionsbedingte Reaktionen
In seltenen Fällen (auch bei der ersten Dosis) wurde ein „Red-Man-Syndrom“ (ein Symptomkomplex bestehend aus Pruritus, Urtikaria, Erythem, angioneurotischem Ödem, Tachykardie, Hypotonie, Dyspnoe) beobachtet.
Das Abbrechen oder Verlangsamen der Infusion kann diese Reaktionen stoppen. Infusionsbedingte Reaktionen können begrenzt sein, wenn die Tagesdosis nicht als Bolusinjektion, sondern als 30-minütige Infusion verabreicht wird.
Schwere bullöse Reaktionen
Bei der Anwendung von Teicoplanin wurden Hautreaktionen wie Stevens-Johnson-Syndrom (SJS) und toxische epidermale Nekrolyse (TEN) berichtet, die den Patienten lebensbedrohlichen oder tödlich verlaufenen ausgesetzt haben. B. fortschreitender Hautausschlag, häufig mit Ulzerationen oder Schleimhautläsionen) sollte die Behandlung mit Teicoplanin sofort beendet werden.
Spektrum der antibakteriellen Aktivität
Teicoplanin hat ein antibakterielles Wirkungsspektrum (Gram positiv) begrenzt. Es ist nicht als Einzelwirkstoff zur Behandlung bestimmter Infektionsarten geeignet, es sei denn, der Erreger ist bereits bekannt und von bekannter Anfälligkeit oder es besteht ein hoher Verdacht, dass der wahrscheinlichste Erreger (die wahrscheinlichsten Erreger) für eine Behandlung (nicht) empfänglich sind mit Teicoplanin.
Die rationelle Anwendung von Teicoplanin muss das antibakterielle Wirkungsspektrum, das Sicherheitsprofil und die Angemessenheit der antibakteriellen Standardtherapie für die Behandlung des einzelnen Patienten berücksichtigen. Auf dieser Grundlage wird erwartet, dass Teicoplanin in vielen Fällen zur Behandlung schwerer Infektionen bei Patienten angewendet wird, für die eine antibakterielle Standardtherapie als ungeeignet erachtet wird.
Ladedosis-Schema
Da nur begrenzte Sicherheitsdaten vorliegen, sollten Patienten engmaschig auf Nebenwirkungen überwacht werden, wenn Teicoplanin-Dosen von 12 mg/kg Körpergewicht zweimal täglich verabreicht werden. Bei diesem Schema sollten zusätzlich zu den empfohlenen regelmäßigen hämatologischen Kontrollen die Kreatininwerte im Blut überwacht werden.
Teicoplanin darf nicht intraventrikulär verabreicht werden.
Thrombozytopenie
Unter Teicoplanin wurde über Thrombozytopenie berichtet. Während der Behandlung werden regelmäßige hämatologische Untersuchungen einschließlich eines großen Blutbildes empfohlen.
Nephrotoxizität
Bei Patienten, die mit Teicoplanin behandelt wurden, wurde über Nierenversagen berichtet (siehe Abschnitt 4.8). Patienten mit Niereninsuffizienz und/oder die Teicoplanin zusammen oder nacheinander mit anderen Arzneimitteln mit bekannter potenzieller Nephrotoxizität (Aminoglykoside, Colistin, Amphotericin B, Ciclosporin und Cisplatin) erhalten, sollten engmaschig überwacht und Hörtests eingeschlossen werden.
Da Teicoplanin hauptsächlich über die Nieren ausgeschieden wird, sollte die Teicoplanin-Dosis bei Patienten mit Niereninsuffizienz angepasst werden (siehe Abschnitt 4.2).
Ototoxizität
Wie bei anderen Glykopeptiden wurde bei mit Teicoplanin behandelten Patienten über Ototoxizität (Taubheit und Tinnitus) berichtet (siehe Abschnitt 4.8). Patienten, die während der Behandlung mit Teicoplanin Anzeichen und Symptome von Hörstörungen oder Innenohrerkrankungen entwickeln, sollten sorgfältig überwacht und untersucht werden, insbesondere bei längerer Behandlung und bei Patienten mit Niereninsuffizienz. Patienten, die Teicoplanin zusammen oder nacheinander mit anderen Arzneimitteln mit bekannter potenzieller Neurotoxizität/Ototoxizität (Aminoglykoside, Ciclosporin, Cisplatin, Furosemid und Ethacrynsäure) erhalten, sollten engmaschig überwacht und bei einer Verschlechterung des Hörvermögens der Nutzen von Teicoplanin bewertet werden.
Besondere Vorsicht ist geboten, wenn Teicoplanin an Patienten verabreicht wird, die eine gleichzeitige Behandlung mit ototoxischen und/oder nephrotoxischen Arzneimitteln benötigen, für die regelmäßige hämatologische Tests und eine Beurteilung der Leber- und Nierenfunktion empfohlen werden.
Superinfektion
Wie bei anderen Antibiotika kann die Anwendung von Teicoplanin insbesondere bei längerer Behandlung das Wachstum nicht empfindlicher Organismen verursachen.Sollte während der Therapie eine Superinfektion auftreten, sollten geeignete Maßnahmen ergriffen werden.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen
Es wurden keine spezifischen Interaktionsstudien durchgeführt.
Teicoplanin- und Aminoglykoside-Lösungen sind inkompatibel und sollten nicht zur Injektion gemischt werden, sie sind jedoch mit Dialyseflüssigkeiten kompatibel und können bei der Behandlung von CAPD-bedingter Peritonitis frei verwendet werden.
Teicoplanin sollte bei gleichzeitiger oder anschließender Therapie mit Arzneimitteln mit bekanntem nephrotoxischem oder ototoxischem Potenzial mit Vorsicht angewendet werden. Dazu gehören Aminoglykoside, Colistin, Amphotericin B, Ciclosporin, Cisplatin, Furosemid und Ethacrynsäure (siehe Abschnitt 4.4). Es gibt jedoch keine Hinweise auf eine synergistische Toxizität in Kombination mit Teicoplanin.
In klinischen Studien wurde Teicoplanin vielen Patienten verabreicht, die bereits verschiedene Arzneimittel erhielten, darunter andere Antibiotika, Antihypertensiva, Anästhetika, Herz-Kreislauf- und Antidiabetika, ohne dass Nebenwirkungen nachgewiesen wurden.
Kinder und Jugendliche
Interaktionsstudien wurden nur bei Erwachsenen durchgeführt.
04.6 Schwangerschaft und Stillzeit
Schwangerschaft
Es liegen nur begrenzte Daten zur Anwendung von Teicoplanin bei schwangeren Frauen vor.Tierstudien haben eine Reproduktionstoxizität bei hohen Dosen gezeigt (siehe Abschnitt 5.3): Bei Ratten kam es zu einer erhöhten Inzidenz von Totgeburten und Neugeborenensterblichkeit. Das potenzielle Risiko für den Menschen ist nicht bekannt. Daher sollte Teicoplanin während der Schwangerschaft nicht angewendet werden, es sei denn, dies ist eindeutig erforderlich. Ein potenzielles Risiko einer Nieren- und Innenohrschädigung des Fötus kann nicht ausgeschlossen werden (siehe Abschnitt 4.4).
Fütterungszeit
Es ist nicht bekannt, ob Teicoplanin beim Menschen in die Muttermilch übergeht. Es liegen keine Informationen über die Ausscheidung von Teicoplanin in die Muttermilch bei Tieren vor.Die Entscheidung, ob das Stillen fortgesetzt/abgesetzt oder die Behandlung mit Teicoplanin fortgesetzt/abgesetzt wird, muss unter Berücksichtigung des Nutzens des Stillens für das Kind und des Nutzens der Teicoplanin-Therapie für die Mutter.
Fruchtbarkeit
Reproduktionsstudien an Tieren haben keine Hinweise auf eine verminderte Fertilität ergeben.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen
Targosid beeinträchtigt leicht die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Teicoplanin kann Schwindel und Kopfschmerzen verursachen. Die Verkehrstüchtigkeit oder die Fähigkeit zum Bedienen von Maschinen kann daher beeinträchtigt sein. Patienten, bei denen solche Nebenwirkungen aufgetreten sind, sollten kein Fahrzeug führen oder Maschinen bedienen.
04.8 Nebenwirkungen
Tabelle der Nebenwirkungen
Die folgende Tabelle listet alle Nebenwirkungen auf, die mit einer höheren Inzidenz als Placebo und bei mehr als 1 Patienten gemäß der folgenden Konvention auftraten:
sehr häufig (≥ 1/10), häufig (≥ 1/100,
Innerhalb der verschiedenen Häufigkeitsgruppen werden Nebenwirkungen nach abnehmendem Schweregrad berichtet.
Nebenwirkungen sollten überwacht werden, wenn Teicoplanin-Dosen von 12 mg/kg Körpergewicht zweimal täglich verabreicht werden (siehe Abschnitt 4.4).
Meldung von vermuteten Nebenwirkungen
Die Meldung vermuteter Nebenwirkungen, die nach der Zulassung des Arzneimittels aufgetreten sind, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden. "Adresse https: //www.aifa.gov.it/content/segnalazioni-reazioni-avverse.
04.9 Überdosierung
Symptome
Es gibt Berichte über fälschlicherweise verabreichte Überdosierungen an pädiatrische Patienten. In einem Fall wurde bei einem 29 Tage alten Säugling, der 400 mg intravenös (95 mg/kg) erhielt, über Unruhe berichtet.
Behandlung
Im Falle einer Überdosierung von Teicoplanin sollte die Behandlung symptomatisch erfolgen.
Teicoplanin wird durch Hämodialyse nicht und nur langsam durch Peritonealdialyse aus dem Kreislauf entfernt.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN
05.1 Pharmakodynamische Eigenschaften
Pharmakotherapeutische Gruppe: Glykopeptid-Antibiotika. ATC-Code: J01XA02.
Wirkmechanismus
Teicoplanin hemmt das Wachstum empfindlicher Mikroorganismen, indem es die Zellwandbiosynthese an einer anderen Stelle als der Zielstelle der Beta-Lactame stört.
Die Synthese von Peptidoglykanen wird durch spezifische Bindung mit den D-Alanyl-D-Alanin-Resten blockiert.
Widerstandsmechanismus
Resistenzen gegen Teicoplanin können auf folgenden Mechanismen beruhen:
• geänderte Zielstruktur: Diese Form des Widerstands trat insbesondere bei der „Enterococcus faecium. Die Modifikation beruht auf der Substitution der Endgruppe D-Alanin-D-Alanin der Aminosäurekette in einer Vorstufe von Murein durch D-Ala-D-Lactat mit daraus resultierender Verringerung der Affinität zu Vancomycin D-Lactat-Dehydrogenase oder neu synthetisierte Ligasen.
• Die verringerte Empfindlichkeit oder Resistenz von Staphylokokken gegenüber Teicoplanin beruht auf einer Überproduktion von Vorläufern des Mureins, an das Teicoplanin bindet.
Es kann zu Kreuzresistenzen zwischen Teicoplanin und dem Glykoprotein Vancomycin kommen. Mehrere Vancomycin-resistente Enterokokken sind empfindlich gegenüber Teicoplanin (Van-B-Phänotyp).
Anfälligkeit - Breakpoint-Werte
Die folgende Tabelle zeigt die Grenzwerte der minimalen Hemmkonzentration (MHK), die empfindliche von resistenten Organismen gemäß EUCAST (European Committee on Antimicrobial Susceptibility Testing) Version 3.1, 11. Februar 2013 trennen:
zu Die MHKs der Glykopeptide sind methodenabhängig und müssen durch Mikroverdünnung der Brühe bestimmt werden (Referenz ISO 20776). S. aureus mit Vancomycin-MHKs von 2 mg/l liegt sie am Extrem der Wildtyp-MHK-Verteilung und es kann zu einem beeinträchtigten klinischen Ansprechen kommen S. aureus wurde auf 2 mg/l reduziert, um die Meldung von intermediären GISA-Isolaten zu vermeiden, da schwere Infektionen mit GISA-Isolaten mit höheren Dosen von Vancomycin oder Teicoplanin nicht behandelbar sind.
B Isolate mit MHK-Werten oberhalb des Empfindlichkeitsgrenzwertes sind sehr selten oder noch nicht gemeldet.Die Tests zur Identifizierung und antimikrobiellen Empfindlichkeit eines solchen Isolats müssen wiederholt werden, und wenn das Ergebnis bestätigt wird, muss das Isolat an ein Referenzlabor geschickt werden. Solange kein Hinweis auf ein klinisches Ansprechen für bestätigte Isolate mit MHK über den aktuellen Grenzwerten vorliegt, sollten solche Isolate als resistent gemeldet werden.
C EI weist darauf hin, dass es keine ausreichenden Beweise dafür gibt, dass die Zielspezies ein gutes Ziel für eine medikamentöse Therapie ist.
D Ein MHK kann mit einem Kommentar gemeldet werden, jedoch nicht mit einer S-, I- oder R-Kategorisierung
Pharmakokinetische / pharmakodynamische Beziehung
Die antimikrobielle Wirkung von Teicoplanin hängt im Wesentlichen davon ab, wie lange die Substanzspiegel über der MHK des Erregers liegen.
Anfälligkeit
Die Prävalenz erworbener Resistenzen kann bei ausgewählten Arten geografisch und zeitlich variieren, daher sind lokale Informationen über Resistenzen wünschenswert, insbesondere bei der Behandlung schwerer Infektionen.
Gegebenenfalls sollte ein Experte hinzugezogen werden, wenn die lokale Prävalenz von Resistenzerscheinungen, zumindest bei einigen Infektionsarten, den Nutzen von Teicoplanin in Frage stellt.
Häufig empfindliche Arten
Aerobe grampositive Bakterien
Corynebacterium jeikeima
Enterococcus faecalis
Staphylococcus aureus (einschließlich Methicillin-resistente Stämme)
Streptococcus agalactiae
Streptokokken-DysGalaktien Untersp. equisimilisa
(Streptokokken der Gruppen C und G)
Streptococcus pneumoniae
Streptococcus pyogenes
Streptokokken der Viridans-Gruppe ein b
Gram-positive anaerobe Bakterien
Clostridium difficile
Peptostreptococcus sppa.
Arten, für die erworbene Ausdauer ein Problem sein kann
Aerobe grampositive Bakterien
Enterococcus faecium
Staphylococcus epidermidis
Staphylococcus haemolyticus
Staphylococcus hominis
Von Natur aus resistente Stämme
Alle gramnegativen Bakterien
Andere Bakterien
Chlamydien spp.
Chlamydophila spp.
Legionella pneumophila
Mykoplasmen spp.
zu Zum Zeitpunkt der Veröffentlichung der Tabelle lagen keine aktualisierten Daten vor. Die Hauptliteratur, Standardtexte und Behandlungsempfehlungen halten es für sensibel.
B Sammelbezeichnung für eine heterogene Gruppe von Streptococcus-Arten. Die Resistenzrate kann je nach tatsächlicher Streptococcus-Art variieren
05.2 Pharmakokinetische Eigenschaften
Absorption
Teicoplanin wird parenteral (intravenös oder intramuskulär) verabreicht. Nach intramuskulärer Gabe ist die Bioverfügbarkeit von Teicoplanin (relativ zur intravenösen Gabe) nahezu vollständig (90%). Nach 6 täglichen intramuskulären Verabreichungen von 200 mg beträgt die mittlere (SD) maximale Konzentration (Cmax) von Teicoplanin 12,1 mg/l und wird 2 Stunden nach der Verabreichung erreicht.
Nach einer intravenös verabreichten Aufsättigungsdosis von 6 mg / kg alle 12 Stunden für 3-5 Verabreichungen liegen die Cmax-Werte zwischen 60 und 70 mg / L und die Cmin-Werte liegen im Allgemeinen über 10 mg / L.
Nach einer Aufsättigungsdosis von 12 mg / kg, die alle 12 Stunden für 3 Verabreichungen intravenös verabreicht wurde, werden die Mittelwerte von Cmax und Cmin auf ungefähr 100 mg / L bzw. 20 mg / L geschätzt.
Nach einer einmal täglich verabreichten Erhaltungsdosis von 6 mg/kg betragen die Cmax- und Cmin-Werte ca. 70 mg/l bzw. 15 mg/l.
Nach einer Erhaltungsdosis von 12 mg/kg einmal täglich liegen die Cmin-Werte im Bereich von 18 bis 30 mg/L.
Teicoplanin wird nach oraler Verabreichung nicht aus dem Magen-Darm-Trakt resorbiert. Nach oraler Gabe einer Einzeldosis von 250 oder 500 mg an gesunde Probanden wurde Teicoplanin nicht im Serum oder Urin, sondern nur in den Fäzes (ca. 45 % der verabreichten Dosis) als unverändertes Arzneimittel wiedergefunden.
Verteilung
Die Proteinbindung im Humanserum reicht von 87,6 bis 90,8 % ohne Variation als Funktion der Teicoplaninkonzentration. Teicoplanin wird hauptsächlich an Serumalbumin gebunden Teicpolanin wird nicht in den roten Blutkörperchen verteilt.
Das Verteilungsvolumen im Steady-State (Vss) reicht von 0,7 bis 1,4 ml/kg. Die höchsten Vss-Werte wurden in neueren Studien beobachtet, bei denen die Probenahmedauer mehr als 8 Tage betrug.
Das Medikament wird hauptsächlich in Lunge, Myokard und Knochengewebe mit Gewebe/Serum-Verhältnissen von mehr als 1 verteilt. In Blasenflüssigkeit, Synovialflüssigkeit und Peritonealflüssigkeit variiert das Gewebe/Serum-Verhältnis von 0,5 bis 1. Die Elimination von Teicoplanin aus der Peritonealflüssigkeit erfolgt mit der gleichen Rate wie aus Serum In Pleuraflüssigkeit und subkutanem Fettgewebe liegt das Gewebe/Serum-Verhältnis zwischen 0,2 und 0,5 Teicoplanin dringt nicht ohne weiteres in die Liquor (CSF) ein.
Biotransformation
Die in Plasma und Urin identifizierte Hauptverbindung ist die unveränderte Form von Teicoplanin, was auf eine minimale Metabolisierung hinweist. Zwei Metaboliten werden wahrscheinlich durch Hydroxylierung gebildet, die 2-3% der verabreichten Dosis ausmachen.
Beseitigung
Unverändertes Teicoplanin wird hauptsächlich über den Urin ausgeschieden (80 % innerhalb von 16 Tagen), während 2,7 % der verabreichten Dosis innerhalb von 8 Tagen nach der Verabreichung in den Fäzes (über die Galle) wiedergefunden werden bis 35 Tage beträgt die Eliminationshalbwertszeit von Teicoplanin 100 bis 170 Stunden.
Teicoplanin hat eine niedrige Gesamtausscheidung in der Größenordnung von 10–14 ml/h/kg und eine renale Elimination in der Größenordnung von 8–12 ml/h/kg, was darauf hinweist, dass Teicoplanin hauptsächlich über die Niere ausgeschieden wird.
Linearität
Teicoplanin weist über einen Dosisbereich von 2 bis 25 mg/kg eine lineare Pharmakokinetik auf.
Besondere Bevölkerungsgruppen
• Nierenversagen
Da Teicoplanin über die Niere eliminiert wird, nimmt die Elimination von Teicoplanin in Abhängigkeit vom Grad der Niereninsuffizienz ab Die Gesamt- und die renale Clearance von Teicoplanin sind abhängig von der Kreatinin-Clearance.
• Ältere Patienten
Bei älteren Patienten ist die Pharmakokinetik von Teicoplanin außer bei Niereninsuffizienz unverändert.
• Kinder und Jugendliche
Im Vergleich zu erwachsenen Patienten besteht eine höhere Gesamtclearance (15,8 ml/h/kg bei Neugeborenen, 14,8 ml/h/kg bei einem Durchschnittsalter von 8 Jahren) und eine kürzere Eliminationshalbwertszeit (40 Stunden bei Säuglingen, 58 Stunden .). bis 8 Jahre).
05.3 Präklinische Sicherheitsdaten
Nach wiederholter parenteraler Gabe wurden bei Ratten und Hunden Wirkungen auf die Niere beobachtet, die sich als dosisabhängig und reversibel erwiesen. Studien zur Untersuchung der potentiellen Ototoxizität beim Meerschweinchen weisen auf die Möglichkeit eines leichten Defizits der Cochlea- und Vestibularisfunktion ohne morphologische Schäden hin.
Subkutan verabreichtes Teicoplanin bis zu 40 mg / kg / Tag veränderte bei Ratten die männliche und weibliche Fertilität nicht.
In Studien zur embryo-fetalen Entwicklung wurden nach subkutaner Gabe von bis zu 200 mg/kg/Tag bei Ratten und intramuskulärer Gabe von bis zu 15 mg/kg/Tag bei Kaninchen keine Missbildungen beobachtet. Bei Ratten kam es jedoch bei Dosierungen ab 100 mg / kg / Tag und darüber zu einer erhöhten Inzidenz von Totgeburten und ab 200 mg / kg / Tag für die neonatale Sterblichkeit.Dieser Effekt wurde bei 50 mg / Tag nicht beobachtet .
Eine Peri- und Postnatalitätsstudie an Ratten zeigte nach subkutaner Gabe von bis zu 40 mg/kg/Tag weder Auswirkungen auf die Fertilität der F1-Generation noch auf die Entwicklung und das Überleben der F2-Generation.
Teicoplanin zeigte kein Potenzial, Antigenität (bei Mäusen, Meerschweinchen oder Kaninchen), Genotoxizität oder lokale Reizung zu verursachen.
06.0 PHARMAZEUTISCHE INFORMATIONEN
06.1 Hilfsstoffe
Pulver zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen
Natriumchlorid
Natriumhydroxid (zur pH-Einstellung)
Lösungsmittel
Wasser für Injektionen.
06.2 Inkompatibilität
Teicoplanin- und Aminoglykoside-Lösungen sind beim direkten Mischen nicht kompatibel und sollten vor der Injektion nicht gemischt werden.
Wird Teicoplanin in Kombinationstherapie mit anderen Antibiotika verabreicht, müssen die Präparate separat verabreicht werden.
Dieses Arzneimittel darf nicht mit anderen Arzneimitteln gemischt werden, außer mit den in Abschnitt 6.6 aufgeführten.
06.3 Gültigkeitsdauer
Gültigkeit des Pulvers in der Verkaufsverpackung
3 Jahre.
Haltbarkeit der rekonstituierten Lösung
Die chemisch-physikalische Stabilität der gemäß den Empfehlungen hergestellten rekonstituierten Lösung wurde für 24 Stunden bei einer Temperatur zwischen 2 und 8 ° C nachgewiesen.
Aus mikrobiologischer Sicht sollte das Produkt sofort verwendet werden. Bei nicht sofortiger Verwendung ist der Benutzer für die Haltbarkeit und die Bedingungen des Produkts verantwortlich, die normalerweise 24 Stunden bei 2 bis 8 ° C nicht überschreiten sollten, es sei denn, die Rekonstitution wird unter kontrollierten Bedingungen durchgeführt und durch Asepsis validiert.
Haltbarkeit des verdünnten Arzneimittels
Die chemisch-physikalische Stabilität der gemäß den Empfehlungen hergestellten rekonstituierten Lösung wurde für 24 Stunden bei einer Temperatur zwischen 2 und 8 ° C nachgewiesen.
Aus mikrobiologischer Sicht sollte das Produkt sofort verwendet werden. Bei nicht sofortiger Verwendung ist der Benutzer für die Haltbarkeit und die Bedingungen des Produkts verantwortlich, die normalerweise 24 Stunden bei 2 bis 8 ° C nicht überschreiten sollten, es sei denn, die Rekonstitution wird unter kontrollierten Bedingungen durchgeführt und durch Asepsis validiert.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung
Pulver in Einzelhandelsverpackungen
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Lagerbedingungen des rekonstituierten/verdünnten Arzneimittels siehe Abschnitt 6.3.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks
Erstverpackung:
Das lyophilisierte Arzneimittel ist verpackt in:
Farblose Durchstechflaschen aus Typ-I-Glas mit einem Nutzvolumen von 10 ml für 200 mg, verschlossen mit einem Brombutyl-Gummistopfen, einer gelben Aluminiumkappe und einer Abreißlasche aus Kunststoff.
Farblose Durchstechflaschen aus Typ-I-Glas mit einem Nutzvolumen von 22 ml für 400 mg, verschlossen mit einem Brombutyl-Gummistopfen, einer grünen Aluminiumkappe und einer Abreißlasche aus Kunststoff.
Das Wasser für Injektionszwecke ist in einer farblosen Typ-I-Glasampulle verpackt.
Pakete:
• 1 Durchstechflasche Pulver mit 1 Durchstechflasche Lösungsmittel
Es werden möglicherweise nicht alle Packungsgrößen in den Verkehr gebracht.
06.6 Gebrauchs- und Handhabungshinweise
Dieses Arzneimittel ist nur zur einmaligen Anwendung bestimmt.
Zubereitung der rekonstituierten Lösung:
• Injizieren Sie langsam den gesamten Inhalt der Durchstechflasche mit dem Lösungsmittel in die Durchstechflasche mit dem Pulver
• Schwenken Sie die Durchstechflasche vorsichtig zwischen Ihren Händen, bis sich das Pulver vollständig aufgelöst hat. Wenn die Lösung schaumig wird, lassen Sie sie etwa 15 Minuten einwirken. Es sollten nur klare und gelbliche Lösungen verwendet werden.
Die rekonstituierten Lösungen enthalten 200 mg Teicoplanin in 3,0 ml und 400 mg in 3,0 ml.
Die rekonstituierte Lösung kann direkt injiziert oder alternativ weiter verdünnt oder oral verabreicht werden.
Zubereitung der verdünnten Lösung vor der Infusion:
Targocid kann in folgenden Infusionslösungen verabreicht werden:
- Natriumchloridlösung 9 mg / ml (0,9%)
- Ringer-Lösung
- Ringer-Laktat-Lösung
• 5% Dextroselösung
• 10 % Dextroselösung
• Lösung mit 0,18 % Natriumchlorid und 4 % Glucose
• Lösung mit 0,45% Natriumchlorid und 5% Glucose
• Peritonealdialyselösung mit 1,36% oder 3,86% Glucoselösung.
Nicht verwendete Arzneimittel und Abfälle aus diesem Arzneimittel müssen gemäß den örtlichen Vorschriften entsorgt werden.
07.0 INHABER DER MARKETING-ERLAUBNIS
Sanofi S.p.A. - Viale L. Bodio, 37 / B - 20158 Mailand
08.0 NUMMER DER MARKETING-ERLAUBNIS
TARGOSID 200 mg Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen
- 1 Durchstechflasche Pulver mit 1 Durchstechflasche A.I.C. n. 026458012
TARGOSID 400 mg Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen
- 1 Durchstechflasche Pulver mit 1 Durchstechflasche A.I.C. n. 026458024
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG
TARGOSID 200 mg Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen
30. Juli 1987/12. September 2013
TARGOSID 400 mg Pulver und Lösungsmittel zur Herstellung einer Injektions-/Infusionslösung oder Lösung zum Einnehmen
13. Februar 2009/12. September 2013
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs
Oktober 2015
11.0 BEI FUNKDRUCK VOLLSTÄNDIGE DATEN ZUR INTERNEN STRAHLENDOSIMETRIE
12.0 FÜR FUNKDROGEN, ZUSÄTZLICHE DETAILLIERTE ANWEISUNGEN ZUR BEISPIELHAFTEN ZUBEREITUNG UND QUALITÄTSKONTROLLE



















.jpg)