Was ist Litak?
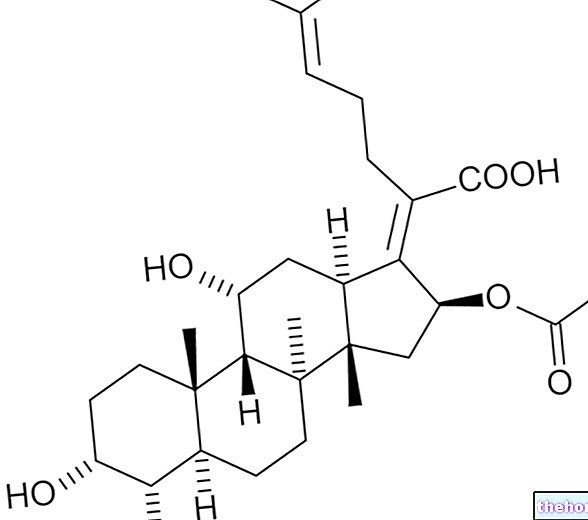
Litak ist eine Injektionslösung, die den Wirkstoff Cladribin enthält.
Wofür wird Litak verwendet?
Litak wird zur Behandlung von Erwachsenen mit Haarzell-Leukämie verwendet, einem Blutkrebs, der durch eine „Überproduktion von B-Lymphozyten (einer Art von weißen Blutkörperchen) verursacht wird. Der Begriff „Haarzellen“ bezieht sich auf Beulen, die wie Haare aussehen. unter dem Mikroskop beobachtbar auf die Oberfläche von Lymphozyten.
Aufgrund der geringen Zahl von Patienten mit Haarzell-Leukämie gilt die Krankheit als selten und Litak wurde am 18. September 2001 als Arzneimittel für seltene Leiden (Arzneimittel für seltene Krankheiten) ausgewiesen.
Das Arzneimittel ist nur auf ärztliche Verschreibung erhältlich.
Wie wird Litak verwendet?
Die Behandlung mit Litak sollte von einem Arzt eingeleitet werden, der Erfahrung in der Krebsbehandlung hat. Litak wird unter die Haut gespritzt. Die empfohlene Dosis beträgt 0,14 mg pro Kilogramm Körpergewicht und wird fünf Tage lang einmal täglich eingenommen. Der Patient kann sich bei entsprechender Schulung selbst injizieren. Litak sollte nicht an Patienten mit mittelschweren bis schweren Leber- oder Nierenproblemen verabreicht werden. Bei Patienten über 65 Jahren sollte es mit Vorsicht und unter häufigen Kontrollen von Leber, Nieren und Blutbild angewendet werden .
Wie funktioniert Litak?
Cladribin, der Wirkstoff in Litak, ist ein zytotoxisches Arzneimittel, ein Arzneimittel, das sich teilende Zellen wie Krebszellen abtöten kann und zu einer Klasse von Arzneimitteln gegen Krebs gehört, die als „Antimetaboliten“ bezeichnet werden. Cladribin ist ein "Analog" von Purin (eine Substanz, deren chemische Struktur der von Purin ähnelt). Purin ist eine der Grundchemikalien, aus denen die DNA besteht. Im Körper wird Cladribin in Lymphozyten in eine chemische Substanz, CdATP, umgewandelt, die an der Bildung neuer DNA beteiligt ist.Dies verhindert die Zellteilung und verlangsamt das Fortschreiten der Leukämie.CdATP kann auch andere Zellen, insbesondere andere Blutzellen, beeinflussen. Cladribin wird seit den 1980er Jahren in Arzneimitteln gegen Krebs eingesetzt und ist in einigen Mitgliedstaaten der Europäischen Union (EU) seit 1993 als intravenöse Infusion (Tropf in eine Vene) erhältlich.
Wie wurde Litak untersucht?
Da Cladribin seit Jahren im Einsatz ist, legte das Unternehmen bereits in der medizinischen Literatur veröffentlichte Daten vor. Litak wurde in einer Hauptstudie mit 63 Erwachsenen mit Haarzell-Leukämie untersucht. In dieser Studie wurde Litak nicht mit anderen Behandlungen verglichen. Der Hauptindikator für die Wirksamkeit war die Anzahl der Patienten, bei denen es nach der Behandlung eine vollständige oder teilweise Remission aufwies. Eine vollständige Remission bedeutet das Verschwinden jeglicher Krankheitszeichen, während eine partielle Remission eine Verbesserung des Blutbildes und eine Verringerung der Anzahl von Krebszellen bedeutet.
Welchen Nutzen hat Litak während der Studien gezeigt?
In der Hauptstudie hatten 97 % der Patienten eine vollständige oder teilweise Remission (60 von 62) und 76 % eine komplette Remission (47 von 62). Diese Ergebnisse ähneln denen, die in anderen veröffentlichten Studien zur intravenösen Anwendung von Cladribin gefunden wurden, und sind besser als die Ergebnisse, die mit alternativen Behandlungen wie Interferon alfa und Pentostatin erzielt wurden.
Welches Risiko ist mit Litak verbunden?
Sehr häufige Nebenwirkungen von Litak (beobachtet bei mehr als 1 von 10 Patienten) sind Infektionen, Panzytopenie oder Myelosuppression (niedrige Anzahl von Blutkörperchen), Purpura (Hautläsion), Immunsuppression (Schwächung des Immunsystems), verminderter Blutdruck. Appetit, Kopfschmerzen, Schwindel, ungewöhnliche Atem- und Brustgeräusche, Husten, Übelkeit, Erbrechen, Verstopfung, Durchfall, Hautausschlag, lokalisierter Hautausschlag (Hautausschlag), Schwitzen (übermäßiges Schwitzen), Reaktionen an der Injektionsstelle (Schmerzen und Entzündungen an der Injektionsstelle), Fieber , Müdigkeit, Schüttelfrost und Asthenie (Schwäche) Die vollständige Liste der von Litak berichteten Nebenwirkungen finden Sie in der Packungsbeilage.
Litak darf nicht bei Patienten angewendet werden, die möglicherweise überempfindlich (allergisch) gegen Cladribin oder einen der sonstigen Bestandteile sind. Litak darf nicht während der Schwangerschaft oder Stillzeit, bei Patienten unter 18 Jahren, bei Patienten mit mittelschwerer bis schwerer Nieren- oder Lebererkrankung oder in Kombination mit anderen Arzneimitteln, die die Bildung von Blutkörperchen hemmen, angewendet werden.
Warum wurde Litak zugelassen?
Der Ausschuss für Humanarzneimittel (CHMP) gelangte zu dem Schluss, dass der Nutzen von Litak bei der Behandlung der Haarzell-Leukämie gegenüber den Risiken überwiegt. Der Ausschuss empfahl die Erteilung einer Marktzulassung für Litak.
Erfahre mehr über Litak
Am 14. April 2004 erteilte die Europäische Kommission der Lipomed GmbH eine in der gesamten Europäischen Union gültige „Zulassung für das Inverkehrbringen" für Litak. Die „Zulassung für das Inverkehrbringen" wurde am 14. April 2009 verlängert.
Die Zusammenfassung des Gutachtens des Ausschusses für Arzneimittel für seltene Leiden zu Litak finden Sie hier.
Für die Vollversion des EPAR von Litak klicken Sie hier.
Letzte Aktualisierung dieser Zusammenfassung: 04-2009.
Die auf dieser Seite veröffentlichten Informationen zu Litak - Cladribin können veraltet oder unvollständig sein. Informationen zur korrekten Verwendung dieser Informationen finden Sie auf der Seite Haftungsausschluss und nützliche Informationen.