Die Elementaranalyse von Proteinen ergibt folgende Durchschnittswerte: 55% Kohlenstoff, 7% Wasserstoff und 16% Stickstoff; es ist klar, dass Proteine sich voneinander unterscheiden, aber ihre durchschnittliche Elementzusammensetzung unterscheidet sich kaum von den oben angegebenen Werten .
Konstitutionell sind Proteine Makromoleküle, die aus natürlichen α-Aminosäuren gebildet werden; die Aminosäuren verbinden sich über die Amidbindung, die durch die Reaktion zwischen einer Aminogruppe einer a-Aminosäure und dem Carboxyl einer anderen a-Aminosäure entsteht.
Diese Bindung (-CO-NH-) wird auch Peptidbindung genannt, da sie Peptide (Aminosäuren in Kombination) bindet:
Das erhaltene ist ein Dipeptid, da es aus zwei Aminosäuren besteht. Da ein Dipeptid an einem Ende eine freie Aminogruppe (NH2) und am anderen eine Carboxylgruppe (COOH) enthält, kann es mit einer oder mehreren Aminosäuren reagieren und die Kette sowohl von rechts als auch von links mit derselben Reaktion verlängern oben gesehen.
Die Abfolge der Reaktionen (die übrigens gar nicht so einfach sind) kann sich unendlich fortsetzen: bis ein Polymer namens Polypeptid oder Protein. Die Unterscheidung zwischen Peptiden und Proteinen hängt mit dem Molekulargewicht zusammen: Normalerweise spricht man bei Molekulargewichten über 10.000 von Proteinen.
Das Zusammenbinden von Aminosäuren, um selbst kleine Proteine zu erhalten, ist eine schwierige Aufgabe, obwohl kürzlich ein automatisches Verfahren zur Herstellung von Proteinen aus Aminosäuren entwickelt wurde, das ausgezeichnete Ergebnisse liefert.
Das einfachste Protein besteht daher aus 2 Aminosäuren: Nach internationaler Konvention beginnt die geordnete Nummerierung der Aminosäuren in einer Proteinstruktur bei der Aminosäure mit der freien a-Aminogruppe.
Codierung für dieses Protein), die auf nicht zu vernachlässigende chemische Schwierigkeiten stößt.
Durch Edman-Abbau konnte die geordnete Sequenz der Aminosäuren bestimmt werden: Das Protein wird mit Phenylisothiocyanat (FITC) umgesetzt, zunächst greift das α-Amino-Stickstoff-Dublett das Phenylisothiocyanat unter Bildung des Thiocarbamyl-Derivats an; anschließend cyclisiert das erhaltene Produkt, was das fluoreszierende Phenylthiohydantoin-Derivat ergibt.
Edman hat eine Maschine namens Sequencer entwickelt, die automatisch die Parameter (Zeit, Reagenzien, pH usw.) für den Abbau anpasst und die Primärstruktur von Proteinen liefert (dafür erhielt er den Nobelpreis).
Die Primärstruktur reicht nicht aus, um die Eigenschaften der Proteinmoleküle vollständig zu interpretieren; Es wird angenommen, dass diese Eigenschaften im Wesentlichen von der räumlichen Konfiguration abhängen, die die Proteinmoleküle annehmen, indem sie sich auf verschiedene Weise falten: dh von der Annahme, was als Sekundärstruktur von Proteinen definiert wurde.
Die Sekundärstruktur von Proteinen flackert, dh sie neigt dazu, sich beim Erhitzen aufzulösen; dann denaturieren sich die Proteine selbst und verlieren viele ihrer charakteristischen Eigenschaften. Neben dem Erhitzen über 70 °C kann eine Denaturierung auch durch Bestrahlung oder durch Einwirkung von Reaktionspartnern (zB von starken Säuren) verursacht werden.
Die Denaturierung von Proteinen durch den thermischen Effekt wird beispielsweise beim Erhitzen des Eiweißes beobachtet: Es verliert sein gallertartiges Aussehen und wird zu einer unlöslichen weißen Substanz. Die Denaturierung von Proteinen führt jedoch zur Zerstörung ihrer Sekundärstruktur, lässt aber ihre Primärstruktur (die Verkettung der verschiedenen Aminosäuren) unverändert.
Proteine nehmen die Tertiärstruktur an, wenn sich ihre Kette, obwohl sie trotz der Biegung der Sekundärstruktur noch flexibel ist, so faltet, dass eine verzerrte dreidimensionale Anordnung in Form eines Festkörpers entsteht. Verantwortlich für die Tertiärstruktur sind vor allem die Disulfidbrücken, die zwischen dem entlang des Moleküls verstreuten Cystein-SH aufgebaut werden können.
Die Quartärstruktur hingegen gehört nur zu Proteinen, die aus zwei oder mehr Untereinheiten bestehen. Hämoglobin zum Beispiel besteht aus zwei Paaren von Proteinen (also in allen vier Proteinketten), die sich an den Ecken eines Tetraeders befinden, so dass eine kugelförmige Struktur entsteht; nicht kovalente Bindungen.
Ein weiteres Beispiel für eine Quartärstruktur ist die von Insulin, die aus bis zu sechs Proteinuntereinheiten zu bestehen scheint, die paarweise an den Eckpunkten eines Dreiecks angeordnet sind, in dessen Zentrum sich zwei Zinkatome befinden.
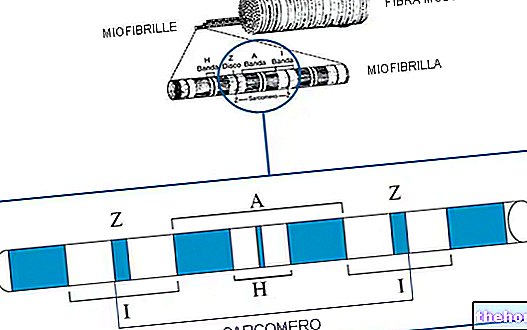
Faserproteine
Sie sind Proteine mit einer gewissen Steifigkeit und einer viel längeren Achse als die anderen; das in der Natur in größeren Mengen vorhandene faserige Protein ist Kollagen (oder Kollagen).
Ein Faserprotein kann verschiedene Sekundärstrukturen annehmen: α-Helix, β-Faltblatt und im Fall von Kollagen Tripelhelix; Die α-Helix ist die stabilste Struktur, gefolgt vom β-Faltblatt, während die am wenigsten stabile der drei die Tripelhelix ist.
rechts wenn nach dem Hauptskelett (von unten nach oben ausgerichtet) eine Bewegung ähnlich dem Eindrehen einer Rechtsschraube ausgeführt wird; während die Helix von . ist linke Hand wenn die Bewegung analog zum Schrauben einer linksgängigen Schraube ist: In den rechten α-Helices stehen die -R-Substituenten der Aminosäuren senkrecht zur Hauptachse des Proteins und zeigen nach außen, während in der linken- Hand a-Helices zeigen die -R-Substituenten nach innen. Rechtshändige a-Helices sind stabiler als linkshändige, da zwischen dem vati-R c "weniger Wechselwirkung und weniger sterische Hinderung besteht. Alle in Proteinen gefundenen a-Helices sind rechtsdrehend.
Die Struktur der α-Helix wird durch die Wasserstoffbrücken (Wasserstoffbrücken) stabilisiert, die zwischen der Carboxylgruppe (-C = O) jeder Aminosäure und der Aminogruppe (-NH) gebildet werden, die vier Reste später im lineare Folge.
Ein Beispiel für ein Protein mit einer α-Helix-Struktur ist Haarkeratin.
Durch Verlängerung der α-Helix-Struktur erfolgt der Übergang von der α-Helix zum β-Faltblatt; auch die Wärme oder die mechanische Spannung ermöglichen den Übergang von der α-Helix zur β-Faltblattstruktur.
Normalerweise liegen die β-Faltblatt-Strukturen in einem Protein nahe beieinander, weil zwischen den Teilen des Proteins selbst Wasserstoffbrückenbindungen zwischen den Ketten aufgebaut werden können.
Bei faserigen Proteinen ist der größte Teil der Proteinstruktur in einer α-Helix oder einem β-Faltblatt organisiert.
Kugelförmige Proteine
Sie haben eine fast kugelförmige Raumstruktur (aufgrund der zahlreichen Richtungsänderungen der Polypeptidkette); einige Teile des Seins lassen sich auf eine α-Helix oder β-Faltblattstruktur zurückführen, andere hingegen sind nicht diesen Formen zuzuschreiben: Die Anordnung ist nicht zufällig, sondern organisiert und repetitiv.
Bei den bisher erwähnten Proteinen handelt es sich um Substanzen von völlig homogener Konstitution: also reine Sequenzen von kombinierten Aminosäuren; solche Proteine werden gesagt einfach; es gibt Proteine, die aus einem Proteinteil und einem Nicht-Proteinteil (Prostatagruppe) bestehen, die Proteine genannt werden konjugieren.
, in den Nägeln, in der Hornhaut und in der Augenlinse, zwischen den Zwischenräumen einiger Organe (zB Leber) und so weiter.
Seine Struktur verleiht ihm besondere mechanische Fähigkeiten; es hat eine hohe mechanische Festigkeit verbunden mit hoher Elastizität (zB in Sehnen) oder hoher Steifigkeit (zB in Knochen) je nach Funktion, die es zu erfüllen hat.
Eine der merkwürdigsten Eigenschaften von Kollagen ist seine konstitutive Einfachheit: Es besteht zu etwa 30 % aus Prolin und etwa 30 % aus Glycin; die anderen 18 Aminosäuren müssen sich nur die restlichen 40% der Proteinstruktur teilen. Die Aminosäuresequenz von Kollagen ist bemerkenswert regelmäßig: Von drei Resten ist der dritte Glycin.
Prolin ist eine cyclische Aminosäure, bei der die R-Gruppe an den α-Aminostickstoff bindet und ihr dadurch eine gewisse Steifigkeit verleiht.
Die Endstruktur ist eine sich wiederholende Kette mit der Form einer "Helix; innerhalb der Kollagenkette fehlen Wasserstoffbrückenbindungen. Kollagen ist eine „linkshändige Helix mit einer Ganghöhe (Länge entsprechend einer Helixwindung) größer als die „α-Helix; die Kollagenhelix ist so locker, dass sich drei Proteinketten umeinander wickeln können und eine „ Einfachseil: Dreifach-Helix-Struktur.
Die Tripelhelix von Kollagen ist jedoch weniger stabil als sowohl die α-Helix als auch die β-Faltblattstruktur.
Sehen wir uns nun den Mechanismus an, durch den Kollagen produziert wird; Denken Sie zum Beispiel an den Riss eines Blutgefäßes: Dieser Riss wird von einer Vielzahl von Signalen begleitet, die darauf abzielen, das Gefäß zu verschließen und so das Gerinnsel zu bilden.
Die Gerinnung erfordert mindestens dreißig spezialisierte Enzyme. Nach dem Gerinnsel ist es notwendig, mit der Reparatur des Gewebes fortzufahren; Zellen in der Nähe der Wunde produzieren auch Kollagen. Dazu wird zunächst die Expression eines Gens induziert, d. h. Organismen, die ausgehend von der Information eines Gens in der Lage sind, das Protein zu produzieren (die genetische Information wird auf die mRNA transkribiert, die den Zellkern verlässt und die Ribosomen im Zytoplasma, wo die genetische Information in Protein übersetzt wird), dann wird das Kollagen in den Ribosomen synthetisiert (es sieht aus wie eine linke Helix, die aus etwa 1200 Aminosäuren besteht und ein Molekulargewicht von etwa 150.000 d hat) und sammelt sich dann in den Lumen an, wo es wird ein Substrat für Enzyme, die in der Lage sind, posttranslationale Modifikationen (Modifikationen der von "mRNA" übersetzten Sprache) durchzuführen; in Kollagen bestehen diese Modifikationen in der Hydroxylierung einiger Seitenketten, insbesondere Prolin und Lysin.
Das Versagen der Enzyme, die zu diesen Veränderungen führen, führt zu Skorbut: Es handelt sich um eine Krankheit, die zunächst zum Bruch von Blutgefäßen, zum Bruch der Zähne, gefolgt von interintestinalen Blutungen und zum Tod führt; es kann durch die kontinuierliche Verwendung von haltbaren Lebensmitteln verursacht werden.
Anschließend treten durch die Wirkung anderer Enzyme weitere Modifikationen auf, die in der Glykosidierung der Hydroxylgruppen von Prolin und Lysin bestehen (ein Zucker bindet an den Sauerstoff des OH); Diese Enzyme befinden sich in anderen Bereichen als dem Lumen, daher wandert das Protein während seiner Modifikationen in das endoplasmatische Retikulum, um in Säcken (Vesikel) zu enden, die sich schließen und sich vom Retikulum lösen: In ihnen ist das glykosidierte Pro . enthalten -Kollagenmonomer; letzteres erreicht den Golgi-Apparat, wo bestimmte Enzyme das im carboxyterminalen Teil des glykosidierten Prokollagens vorhandene Cystein erkennen und die verschiedenen Ketten dazu bringen, sich einander zu nähern und Disulfidbrücken zu bilden: auf diese Weise drei Ketten von Glykosidiertes Pro-Kollagen werden miteinander verbunden erhalten, und dies ist der Ausgangspunkt, von dem die drei Ketten, die sich gegenseitig durchdringen, spontan die Tripelhelix bilden.Die drei miteinander verbundenen Ketten von glykosidiertem Pro-Kollagen erreichen , dann ein Vesikel, das, an sich selbst ersticken, löst sich vom Golgi-Apparat und transportiert die drei Ketten zur Peripherie der Zelle, wo sie durch die Fus Ion mit der Plasmamembran wird das Trimeter aus der Zelle ausgestoßen.
Im extrazellulären Raum gibt es bestimmte Enzyme, die Pro-Kollagen-Peptidasen, die aus der aus der Zelle ausgestoßenen Spezies drei Fragmente (eines für jede Helix) von 300 Aminosäuren entfernen l "eins, aus dem terminalen Carboxyteil und drei Fragmente (eines für jede Helix) von jeweils etwa 100 Aminosäuren, vom aminoterminalen Teil: es verbleibt eine Tripelhelix bestehend aus etwa 800 Aminosäuren pro Helix, bekannt als Tropokollagen.
Tropokollagen hat das Aussehen eines ziemlich starren Stäbchens; die verschiedenen Trimeren verbinden sich mit kovalenten Bindungen zu größeren Strukturen: Mikrofibrillen. In den Mikrofibrillen sind die verschiedenen Trimeren gestaffelt angeordnet; viele Mikrofibrillen bilden Tropokollagenbündel.
In den Knochen gibt es zwischen den Kollagenfasern Zwischenräume, in denen sich Sulfate und Phosphate von Kalzium und Magnesium ablagern: Diese Salze bedecken auch alle Fasern; Dadurch werden die Knochen steif.
In Sehnen sind die Zwischenräume weniger kristallinreich als in Knochen, während kleinere Proteine als in Tropokollagen vorhanden sind: Dies verleiht den Sehnen Elastizität.
Osteoporose ist eine Krankheit, die durch einen Mangel an Kalzium und Magnesium verursacht wird und es unmöglich macht, Salze in den interstitiellen Bereichen der Tropokollagenfasern zu fixieren.