1) PROTEINZIELE
Hier sind einige Beispiele für Protein-Targets. Im ersten Beispiel betrachten wir ein "Hämoprotein, das Hämoglobin ist" und ein sehr ähnliches Gift, das Kohlenmonoxid (CO) ist. Kohlenmonoxid, das dem Sauerstoff 250-mal ähnlicher ist, bindet an die -EME-Gruppe des Hämoglobins und verhindert so den Sauerstofftransport Die Gewebezellen sterben an ANÄMISCHER HYPOXIE, weil sie nicht den für die Zellatmung notwendigen Sauerstoff erhalten.
Im zweiten Beispiel wird ein enzymatisches Proteinmolekül, die Cyt-C-Oxidase, und das verwandte toxische Cyanid betrachtet. Cyt-C-Oxidase ist ein Enzym, das zur Elektronentransportkette gehört. Die Zellatmung findet auf der Ebene des Mitochondriums statt und die Cyt-C-Oxidase nutzt Sauerstoff, um sicherzustellen, dass vier H + -Ionen aus dem Mitochondrium ausgestoßen werden; diese Ausscheidung von Wasserstoffionen bildet die für die Synthese von ATP notwendige Potentialdifferenz. Enzym wird durch Cyanid blockiert , Cyt-C-Oxidase verwendet keinen molekularen Sauerstoff mehr, der optimale Protonengradient bildet sich nicht außerhalb des Mitochondriums; folglich synthetisiert die Zelle kein ATP. Auch in diesem Fall gehen die Zellen dem Tod durch Hypoxie entgegen; wir sprechen insbesondere von CYTOTOXIC HYPOXIA.
Unter all den Protein-Targets finden wir die Rezeptoren, die in der allgemeinen Pharmakologie erklärt wurden. Die wichtigsten Toxine wie Nikotin und Strychnin können mit verschiedenen Rezeptoren interagieren.
2) LIPID-ZIELE
Die am stärksten von freien Radikalen betroffenen Lipide sind die der Membran. Das freie Radikal entsteht aus chemischer Sicht, weil zwischen zwei Atomen keine "Heterolyse" stattfindet, also keine zwei Ionen mit einer homogenen Ladung gebildet werden, sondern es findet eine "Homolyse" statt.
Die Homolyse zeichnet sich durch eine ungleichmäßige Verteilung der Ladungen aus.

Freie Radikale entstehen aus äußeren Stoffen (Xenobiotika), aber auch in unserem Organismus (Sauerstofffreie Radikale). Wir können daher sagen, dass sich sowohl von außen als auch von innen in unserem Organismus freie Radikale bilden können.
Wie entstehen diese Radikale?
Freie Sauerstoffradikale können sich bilden, wenn sich die Sauerstoffpartialspannung in der Zelle ändert, es also zu plötzlichen Änderungen des Sauerstoffdrucks kommt. Dieser plötzliche Sauerstoffmangel begünstigt die Bildung von Radikalspezies im ischämischen (Gehirn) oder Herzgewebe. Die radikalen Sauerstoffspezies stellen hauptsächlich das SUPEROXID-ANION und das OXIDRILE dar. Der Mangel an Antioxidantien (Vitamine A, C und E), die Zellalterung, Xenobiotika und schließlich die akuten und / oder chronischen Entzündungszustände sind alles Phänomene, die zu dem Bildung von freien Radikalen.

Auf diese möglichen Schäden kann die Zelle durch das Einsetzen von freien Sauerstoffradikalen reagieren, da sie über bestimmte Enzyme verfügt, die der Aktivität der Radikale entgegenwirken.

3) ZIELGRUPPEN - SH
Das dritte Ziel sind die SH-Gruppen von Proteinen, die durch freie Sauerstoffradikale oxidiert werden.
Die Proteine, die am meisten durch freie Radikale geschädigt werden, sind:
- Alle zytoskelettalen Proteine, die -SH-Gruppen besitzen, wie Aktin und Tubulin;
- Integrale Proteine der Plasmamembran;
- Alle Membransysteme der Signalübertragung.
- Die Proteine der Mitochondrienmembran;
- ATPase, die das Calciumion aus der Zelle transportiert (die Ansammlung von Calcium in der Zelle führt zum Zelltod);
- Die Proteinkinase C;
Glutathion (GSH) schützt die Zelle vor oxidativem Stress. Glutathion schafft es, die Wirkung von Wasserstoffperoxid dank GPO (Glutathionperoxidase) zu deaktivieren.
Das oxidierte GSH kann wieder reduziert werden, wenn ihm NADPH zur Verfügung steht; wenn kein "NADPH oder c" vorhanden ist, zu viel Wasserstoffperoxid vorhanden ist, kann das GSH nicht in reduzierter Form zurückkehren und ist somit nicht mehr gegen oxidativen Stress funktionsfähig.
4) NUKLEINSÄUREZIELE
Ziel toxischer Substanzen sind Nukleinsäuren, die aus Pyrimidin- und Purin-Basenpaaren gebildet werden. Die xenobiotischen Verbindungen, die als Alkylierungsmittel der Purin- und Pyrimidinbasen wirken, verhindern die Synthese und Replikation des DNA-Strangs. Unter diesen gefährlichen Stoffen finden wir die NITROSAMINEN, die zwischen den Nitriten, die als Konservierungsstoffe in Fleisch- und Wurstwaren verwendet werden, und den sekundären aromatischen Aminen, die aus verschiedenen Kochmethoden stammen, gebildet werden.
Im Magen, wo der pH-Wert sehr sauer ist, reagieren Nitrite und sekundäre aromatische Amine zu Nitrosaminen, deren Funktion für den DNA-Strang sehr gefährlich ist.
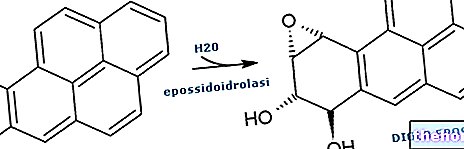
Eine weitere toxische Substanz, die als DNA-Alkylierungsmittel wirkt, ist AFLATOXIN. Letzteres ist ein Mykotoxin, das für die Verschmutzung von Getreide verantwortlich ist. Sobald es in unseren Körper eingedrungen ist, wird es unter Bildung eines Epoxy-Metaboliten metabolisiert, der für die alkylierende Wirkung verantwortlich ist.
Wie sich ableiten lässt, werden Nitrosamine in unserem Körper durch eine Reaktion zwischen zwei durch die Nahrung zugeführten Verbindungen gebildet, während Aflatoxin durch kontaminiertes Getreide in unseren Körper gelangt.
Neben dem Hauptschaden einer falschen DNA-Replikation kann es zu einer möglichen Bildung falscher Basentripletts kommen, die die falschen Aminosäuren synthetisieren. Es kann auch zu einer DNA-Fragmentierung kommen, mit nachfolgender Zerstörung der Moleküle, aus denen die Basen bestehen (Öffnung des Imidazolrings), mit abschließender Bildung des Hydroxylradikals.Mit der Öffnung des Imidazolrings wird die DNA-Replikation blockiert kann zwischen den Basen (CROSSING LINKING) des gleichen Strangs oder komplementärer Stränge entstehen Aufgrund der Bildung dieser Bindungen trennt sich der DNA-Strang während der Replikation nicht.
Zusammenfassend sind die möglichen DNA-Schäden durch toxische Substanzen:
- BILDUNG VON ADDUKTEN (DNA-Alkylierung);
- FRAGMENTIERUNG DER DNA (Öffnung des "Imidazolrings mit Replikationsblock);
- BILDUNG VON GEKREUZTEN BINDUNGEN ZWISCHEN DEN BASES (Fehler beim Öffnen des Filaments während der Replikation).
Mit dem vierten Ziel endet der Teil, in dem die möglichen Ziele der Süchtigen erläutert werden.
Weitere Artikel zum Thema "Zielmoleküle von Giftstoffen"
- Toxikodynamik
- Toxizität und Toxikologie
- Reaktionen zwischen toxischem und biologischem Ziel