Wirkstoffe: Tyrotricin, Cetrimoniobromid, Benzocain
GOLAMIXIN® Spray für Mundschleimhaut
Warum wird Golamixin verwendet? Wofür ist das?
PHARMAKOTHERAPEUTISCHE KATEGORIE
Vorbereitet für die Oropharynxhöhle - ATC R02A
THERAPEUTISCHE HINWEISE
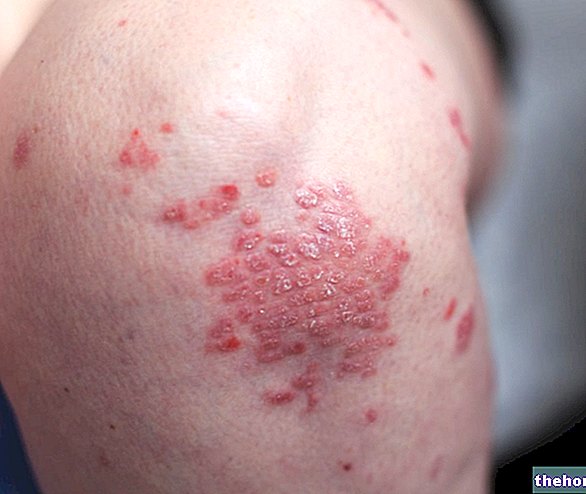
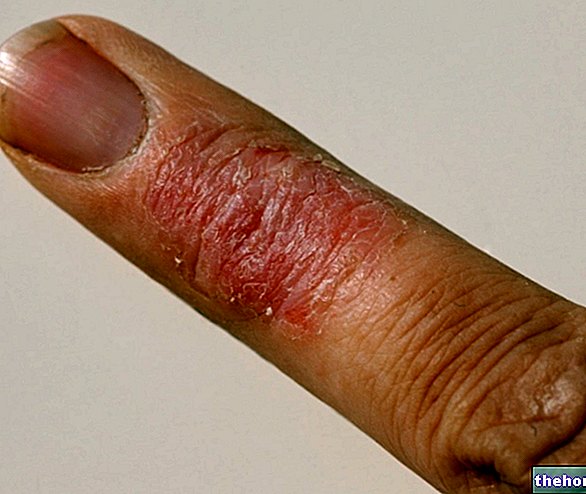
Topische Therapie der thyreotricinempfindlichen bakteriellen Stomatitis.
Kontraindikationen Wenn Golamixin nicht verwendet werden sollte
Patienten mit bekannter Überempfindlichkeit gegen die Bestandteile, insbesondere Thyrotricin.
Patienten, deren ausgeprägte Veranlagung für Allergien bekannt ist.
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Golamixin® beachten?
Bei schwangeren Frauen und in der sehr frühen Kindheit sollte das Tierarzneimittel in dringenden Fällen und unter direkter Aufsicht des Arztes verabreicht werden.
Falls innerhalb von zwei Tagen nach Beginn der Anwendung keine Reaktion eintritt, die Behandlung wegen möglicher Besiedlung mit Thyrotricin-resistenten Bakterienstämmen oder Pilzen (insbesondere Candida) unterbrechen Phänomene. In diesem Fall muss die Therapie unterbrochen und eine geeignete Therapie eingeleitet werden.
Ein ähnliches Verhalten ist bei der Entwicklung unempfindlicher Mikroorganismen zu beachten.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Golamixin® beeinflussen?
Aufgrund der geringen verabreichten Dosen sind keine schwerwiegenden Wechselwirkungen mit anderen Arzneimitteln zu erwarten.
Warnungen Es ist wichtig zu wissen, dass:
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Für diejenigen, die sportliche Aktivitäten ausüben, kann die Einnahme von ethylalkoholhaltigen Arzneimitteln positive Dopingtests in Bezug auf die von einigen Sportverbänden angegebenen Alkoholkonzentrationsgrenzwerte ergeben.
Dosierung und Art der Anwendung Wie ist Golamixin anzuwenden: Dosierung
Erwachsene: 2-3 Anwendungen gleichzeitig, 3-4 mal täglich.
Kinder: 1-2 Anwendungen gleichzeitig, 3-4 mal täglich.
Die Abgabe wird durch ein bestimmtes Dosierventil genau dosiert Drücken Sie die Abwärtstaste, um eine dosierte Abgabe zu erhalten.
Überdosierung Was ist zu tun, wenn Sie zu viel Golamixin eingenommen haben?
Es sind keine Manifestationen einer Überdosierungstoxizität bekannt.
Nebenwirkungen Was sind die Nebenwirkungen von Golamixin?
Bei der Anwendung von Thyrotricin wurde über Zungenschwärzung, selten Glossitis und Sensibilisierungsreaktionen berichtet, die sich jedoch mit Unterbrechung der Behandlung zurückbilden. Relevanter können die Sensibilisierungssymptome von Anästhetika sein, einschließlich Muskelerkrankungen, Krämpfe.
Der Patient wird gebeten, seinem Arzt oder Apotheker jede andere als die oben genannten Nebenwirkungen mitzuteilen.
Ablauf und Aufbewahrung
Golamixin muss an einem kühlen Ort aufbewahrt werden.
Gültigkeit: 36 Monate.
Achtung: Verwenden Sie das Arzneimittel nicht nach dem auf der Packung angegebenen Verfallsdatum.
Frist "> Weitere Informationen
KOMPOSITION
100ml enthalten:
- WIRKSTOFFE: Thyrotricin 0,02 g; Cetrimonbromid 0,05 g; Benzocain g 0,05.
- SONSTIGE BESTANDTEILE: Ätherisches Pfefferminzöl; Alkohol.
PHARMAZEUTISCHES FORMBLATT
"Mundschleimhautspray" Flasche 10 ml.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS -
GOLAMIXIN
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG -
100ml enthalten:
Wirkstoffe: Thyrotricin 0,02 g; Cetrimonbromid 0,05 g; Benzocain g 0,05.
03.0 DARREICHUNGSFORM -
Mundschleimhautspray.
04.0 KLINISCHE INFORMATIONEN -
04.1 Anwendungsgebiete -
Topische Therapie der thyreotricinempfindlichen bakteriellen Stomatitis.
04.2 Dosierung und Art der Anwendung -
Erwachsene: 2-3 Anwendungen gleichzeitig, 3-4 mal täglich.
Kinder: 1-2 Anwendungen gleichzeitig, 3-4 mal täglich.
04.3 Kontraindikationen -
Patienten mit bekannter Überempfindlichkeit gegenüber den einzelnen Bestandteilen, insbesondere Thyrotricin. Patienten, deren ausgeprägte Veranlagung für Allergien bekannt ist.
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung -
In der sehr frühen Kindheit sollte das Tierarzneimittel in dringenden Fällen und unter direkter Aufsicht des Arztes verabreicht werden.
Wenn innerhalb von zwei Tagen nach Beginn der Verabreichung keine Reaktion eintritt, die Behandlung wegen einer möglichen Besiedlung mit Thyrotricin-resistenten Stämmen oder Pilzen (insbesondere Candida) unterbrechen.Die Anwendung topischer Produkte, insbesondere bei längerer Anwendung, kann zu Sensibilisierungserscheinungen führen . In diesem Fall muss die Therapie unterbrochen und eine geeignete Therapie eingeleitet werden. Ein ähnliches Verhalten ist bei der Entwicklung unempfindlicher Mikroorganismen zu beachten.
Außerhalb der Reichweite von Kindern aufbewahren.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen -
Aufgrund der geringen verabreichten Dosen sind keine schwerwiegenden Wechselwirkungen mit anderen Arzneimitteln zu erwarten.
04.6 Schwangerschaft und Stillzeit -
Bei schwangeren Frauen sollte das Produkt in dringenden Fällen und unter direkter Aufsicht des Arztes verabreicht werden.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen -
Die Gabe von Golamixin hat keinen Einfluss auf die Aufmerksamkeitsspanne, daher besteht keine Behinderung beim Führen von Fahrzeugen und beim Bedienen von Präzisionsmaschinen.
04.8 Nebenwirkungen -
Bei der Anwendung von Thyrotricin wurde über Zungenschwärzung, selten Glossitis und Sensibilisierungsreaktionen berichtet, die sich jedoch mit Unterbrechung der Behandlung zurückbilden. Relevanter können die Sensibilisierungssymptome von Anästhetika sein, einschließlich Muskelerkrankungen, Krämpfe.
04.9 Überdosierung -
Es sind keine Manifestationen einer Überdosierungstoxizität bekannt.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN -
05.1 "Pharmakodynamische Eigenschaften -
Golamixin besteht aus der Verbindung des Antibiotikums Thyrotricin mit dem Desinfektionsmittel Cetrimid und dem Lokalanästhetikum Benzocain Die mit Golamixin durchgeführten pharmakologischen Tests haben bestätigt, dass die Spezialität die bereits bekannten Aktivitäten der einzelnen Wirkstoffe besitzt und ausführt Zutaten darin Inhalt.
05.2 "Pharmakokinetische Eigenschaften -
Die in Golamixin enthaltenen Wirkstoffe stören die bakterielle Darmflora nicht und werden vom Körper nicht in solchen Konzentrationen aufgenommen, dass eine systemische mikrobielle Aktivität festgestellt werden könnte.
05.3 Präklinische Daten zur Sicherheit -
Akute Toxizitätstests, die an Ratten und Mäusen auf oralem und subkutanem Weg durchgeführt wurden, lieferten LD50-Werte von mehr als 50 mg / kg bzw. 20 mg / kg, was dem Produkt eine große Sicherheitsspanne verleiht. Die chronische Behandlung über 24 Wochen wurde vom Organismus oral behandelter Ratten und Hunde gut vertragen. Die Behandlung mit Golamixin hatte keinen Einfluss auf die Fertilität von oral behandelten Ratten und Kaninchen, und es zeigte sich auch keine maternale Toxizität und teratogene Wirkung keine nennenswerten akuten Kreislaufwirkungen beim narkotisierten Kaninchen.
06.0 PHARMAZEUTISCHE INFORMATIONEN -
06.1 Hilfsstoffe -
Ätherisches Pfefferminzöl ml 0,25; Alkohol nach Geschmack bei 100ml.
06.2 Inkompatibilität "-
Unverträglichkeiten mit anderen Arzneimitteln sind nicht bekannt.
06.3 Gültigkeitsdauer "-
3 Jahre in intakter Verpackung.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung -
Keiner.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks -
Neutralglasflasche, Typ III, verschlossen mit Dosierpumpe und ausgestattet mit oralem Dispenser.
Sprühen Sie 10 ml
06.6 Gebrauchs- und Handhabungshinweise -
07.0 INHABER DER "MARKETING GENEHMIGUNG" -
Teofarma S.r.l. - über F.lli Cervi, 8 -27010 Valle Salimbene (PV)
08.0 NUMMER DER VERMARKTUNGSBERECHTIGUNG -
Oromucosal Spray 10 ml Flasche - A.I.C. 016703035 -
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG -
Oktober 1960 / Juni 2010
10.0 DATUM DER ÜBERARBEITUNG DES TEXTs -
Juni 2010