Wirkstoffe: Pizotifen (Pizotifen Malatsäure)
Sandomigran 0,5 mg überzogene Tabletten
Indikationen Warum wird Sandomigran angewendet? Wofür ist das?
Sandomigran enthält den Wirkstoff Pizotifen, der zu einer Gruppe von Arzneimitteln gehört, die als Anti-Migräne (Migräne) bezeichnet werden.
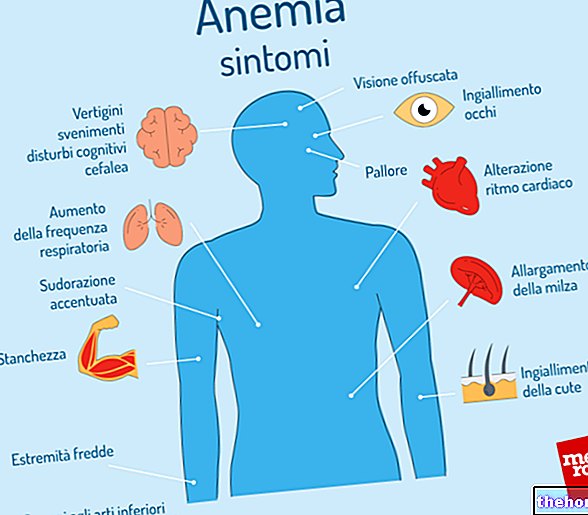
Sandomigran ist angezeigt zur Vorbeugung von wiederkehrenden Kopfschmerzen, die durch Blutgefäßprobleme verursacht werden, wie:
- typische oder atypische Migräne (auch als rezidivierende Migräne mit oder ohne Aura bezeichnet)
- Cluster-Kopfschmerz
Sandomigran ist nicht zur Schmerzstillung während einer Migräneattacke indiziert.
Kontraindikationen Wann Sandomigran nicht angewendet werden sollte
Nehmen Sie Sandomigran nicht ein
- wenn Sie allergisch gegen Pizotifen oder einen der sonstigen Bestandteile dieses Arzneimittels sind (aufgelistet in Abschnitt 6)
- wenn Sie schwanger sind oder stillen (siehe Abschnitt „Schwangerschaft und Stillzeit“)
Sandomigran sollte Kindern unter 2 Jahren nicht verabreicht werden.
Vorsichtsmaßnahmen für die Anwendung Was sollten Sie vor der Einnahme von Sandomigran® beachten?
Bitte sprechen Sie mit Ihrem Arzt oder Apotheker, bevor Sie Sandomigran einnehmen.
Informieren Sie Ihren Arzt vor der Einnahme von Sandomigran:
- wenn Sie Leberprobleme haben oder vermuten, dass Sie diese haben. Ihr Arzt wird regelmäßige Tests durchführen, um Ihre Leberfunktion zu beurteilen
- wenn Sie Nierenprobleme haben
- wenn Sie ein Engwinkelglaukom haben, das nicht operativ behandelt wurde
- wenn Sie unter Harnverhalt leiden, z. bei Prostatahypertrophie
- wenn Sie Epilepsie haben
- wenn bei Ihnen das Risiko besteht, eine Porphyrie genannte Erkrankung zu entwickeln, zum Beispiel wenn Sie diese in der Vergangenheit zusammen mit anderen Arzneimitteln hatten
Seien Sie besonders vorsichtig und informieren Sie Ihren Arzt:
- wenn Sie während der Behandlung mit Sandomigran Anzeichen von Leberproblemen bemerken. Ihr Arzt wird Ihnen sagen, dass Sie die Behandlung abbrechen sollen, bis die Ursache der Leberprobleme geklärt ist
- wenn Sie Sehstörungen bemerken.
Nach abruptem Absetzen von Pizotifen wurde über Entzugserscheinungen wie Depression, Zittern, Übelkeit, Angst, Unwohlsein, Schwindel, Schlafstörungen und Gewichtsverlust berichtet (siehe Abschnitt „Mögliche Nebenwirkungen“). Daher wird ein schrittweises Absetzen der Behandlung mit Sandomigran empfohlen.
Kinder
Sandomigran sollte Kindern unter 2 Jahren nicht verabreicht werden.
Wechselwirkungen Welche Medikamente oder Lebensmittel können die Wirkung von Sandomigran® beeinflussen?
Informieren Sie Ihren Arzt oder Apotheker, wenn Sie andere Arzneimittel anwenden, kürzlich andere Arzneimittel angewendet haben oder beabsichtigen andere Arzneimittel einzunehmen.
Informieren Sie Ihren Arzt, wenn Sie Folgendes anwenden:
- Cisaprid (Arzneimittel zur Behandlung von Magenproblemen)
- adrenerge Blocker (Arzneimittel zur Behandlung von Bluthochdruck)
- Beruhigungsmittel und Hypnotika (Arzneimittel zur Verringerung von Angstzuständen und zur Förderung des Schlafs)
- Antihistaminika (Arzneimittel zur Behandlung von Allergien)
- Monoaminoxidase-Hemmer (Arzneimittel zur Behandlung von Depressionen).
Sandomigran mit Alkohol
Sandomigran verstärkt die Wirkung von Alkohol. Nehmen Sie dieses Arzneimittel daher nicht zusammen mit Alkohol ein.
Warnungen Es ist wichtig zu wissen, dass:
Schwangerschaft und Stillzeit
Wenn Sie schwanger sind oder stillen, oder wenn Sie vermuten, schwanger zu sein oder beabsichtigen, schwanger zu werden, fragen Sie vor der Einnahme dieses Arzneimittels Ihren Arzt oder Apotheker um Rat.
Schwangerschaft
Wenn Sie schwanger sind, wird Ihnen das Arzneimittel nur in dringenden Fällen und unter direkter Aufsicht Ihres Arztes verschrieben.
Fütterungszeit
Verwenden Sie Sandomigran nicht während der Stillzeit.
Verkehrstüchtigkeit und das Bedienen von Maschinen
Dieses Arzneimittel wird Ihre Verkehrstüchtigkeit und Ihre Fähigkeit zum Bedienen von Maschinen beeinträchtigen, da es Schläfrigkeit, Sedierung und Schwindel verursachen kann. Während der Behandlung mit Sandomigran dürfen Sie kein Fahrzeug führen und keine Maschinen bedienen.
Sandomigran enthält Lactose, Saccharose und Erdnussöl
Dieses Arzneimittel enthält Lactose und Saccharose. Bitte nehmen Sie dieses Arzneimittel erst nach Rücksprache mit Ihrem Arzt ein, wenn Ihnen bekannt ist, dass Sie unter einer Zuckerunverträglichkeit leiden. Dieses Arzneimittel enthält Erdnussöl.Verwenden Sie es nicht, wenn Sie allergisch gegen Erdnüsse oder Soja sind.
Dosis, Methode und Zeitpunkt der Anwendung Wie ist Sandomigran anzuwenden: Dosierung
Nehmen Sie dieses Arzneimittel immer genau nach Absprache mit Ihrem Arzt oder Apotheker ein. Fragen Sie im Zweifelsfall Ihren Arzt oder Apotheker.
Erwachsene
Die empfohlene Anfangsdosis beträgt 0,5 mg pro Tag. Ihr Arzt kann die Dosis schrittweise erhöhen.
Die durchschnittliche Erhaltungsdosis beträgt 1,5 mg pro Tag, die in mehreren Dosen über den Tag verteilt oder einmal am Abend verabreicht wird.
Wenn Sandomigran bei diesen Dosen keine Wirkung zeigt, kann Ihr Arzt die Dosis schrittweise auf 3 – 4,5 mg pro Tag in 3 Einzeldosen erhöhen.
Anwendung bei Kindern über zwei Jahren und Jugendlichen
Die empfohlene Anfangsdosis beträgt 0,5 mg pro Tag.
Ihr Arzt kann die Dosis auf 1,5 mg erhöhen, die in mehreren Dosen über den Tag verteilt oder einmal abends eingenommen wird.
Sandomigran sollte Kindern unter 2 Jahren nicht verabreicht werden.
Anwendung bei Patienten mit schweren Nieren- oder Leberproblemen (Nieren- oder Leberversagen)
Wenn Sie an Leber- oder Nierenversagen leiden, wird Ihr Arzt bei der Verschreibung von Sandomigran besondere Vorsicht walten lassen und entscheiden, welche Dosis für Sie am besten geeignet ist.
Wenn Sie die Einnahme von Sandomigran® vergessen haben
Nehmen Sie nicht die doppelte Dosis ein, wenn Sie die vergessene Tablette vergessen haben.
Wenn Sie die Anwendung von Sandomigran abbrechen
Brechen Sie die Einnahme von Sandomigran nicht ohne vorherige Rücksprache mit Ihrem Arzt ab.
Es wird jedoch empfohlen, die Behandlung mit Sandomigran schrittweise abzusetzen, da nach abruptem Absetzen von Pizotifen (dem Wirkstoff in Sandomigran) über Depressionen, Zittern, Übelkeit, Angstzustände, Unwohlsein, Schwindel, Schlafstörungen, Gewichtsverlust und Bewusstlosigkeit berichtet wurde.
Wenn Sie weitere Fragen zur Anwendung dieses Arzneimittels haben, wenden Sie sich an Ihren Arzt oder Apotheker
Überdosierung Was ist zu tun, wenn Sie zu viel Sandomigran® eingenommen haben?
Im Falle einer versehentlichen Einnahme einer Überdosis Sandomigran benachrichtigen Sie sofort Ihren Arzt oder begeben Sie sich in das nächste Krankenhaus.
Wenn Sie zu viel Sandomigran eingenommen haben, können Schläfrigkeit, Übelkeit, Erbrechen, Mundtrockenheit, schneller Herzschlag, Fieber, niedriger Blutdruck, Atembeschwerden, Blaufärbung der Haut und der Schleimhäute, Schwindel, Verwirrtheit, Verlust der Bewegungskoordination, Sedierung, verminderte Aktivität des Zentralnervensystems, Erregungszustand (bei Kindern), verminderte Atemaktivität, Krämpfe (insbesondere bei Kindern), Koma.
Bei Kindern können Halluzinationen, Bewegungskoordinationsstörungen, feste und erweiterte Pupillen, Gesichtsrötung und Fieber auftreten, die bis zum Koma und Kollaps von Herz und Lunge fortschreiten können.
Ihr Arzt wird die Einnahme einer Überdosis Sandomigran entsprechend Ihrem Zustand behandeln.
Nebenwirkungen Was sind die Nebenwirkungen von Sandomigran
Wie alle Arzneimittel kann auch dieses Arzneimittel Nebenwirkungen haben, die aber nicht bei jedem auftreten müssen.
Sehr häufige Nebenwirkungen (kann mehr als 1 von 10 Behandelten betreffen)
- gesteigerter Appetit
- Gewichtszunahme
Häufige Nebenwirkungen (kann bis zu 1 von 10 Behandelten betreffen)
- Sedierung (einschließlich Schläfrigkeit)
- Schwindel
- Brechreiz
- trockener Mund
- Ermüdung
Gelegentliche Nebenwirkungen (kann bis zu 1 von 100 Behandelten betreffen)
- Verstopfung
Seltene Nebenwirkungen (kann bis zu 1 von 1.000 Behandelten betreffen)
- allergische Reaktionen
- Schwellung des Gesichts durch Flüssigkeitsansammlung (Gesichtsödem)
- Depression
- Stimulation des zentralen Nervensystems (z. B. Aggression, Erregung)
- Halluzinationen
- Angst
- Kribbeln
- Hautreaktionen: Nesselsucht und Hautausschlag (Hautausschlag)
- Muskelschmerzen (Myalgie)
Sehr seltene Nebenwirkungen (kann bis zu 1 von 10.000 Behandelten betreffen)
- Krämpfe
Nebenwirkungen mit nicht bekannter Häufigkeit (Häufigkeit auf Grundlage der verfügbaren Daten nicht abschätzbar)
- Anstieg einiger Leberenzyme, die auf Leberprobleme hinweisen
- Gelbfärbung von Haut, Schleimhäuten und Augen (Gelbsucht)
- Leberentzündung (Hepatitis)
- Muskelkrämpfe
Entzugserscheinungen nach abruptem Absetzen von Pizotifen
Nach abruptem Absetzen von Pizotifen wurde über Depression, Zittern, Übelkeit, Angst, Unwohlsein, Schwindel, Schlafstörungen, Gewichtsverlust und Bewusstlosigkeit berichtet.
Meldung von Nebenwirkungen
Wenn Sie Nebenwirkungen bemerken, wenden Sie sich an Ihren Arzt oder Apotheker, einschließlich aller möglichen Nebenwirkungen, die nicht in dieser Packungsbeilage aufgeführt sind. Sie können Nebenwirkungen auch direkt über das nationale Meldesystem unter http://www.agenziafarmaco.gov.it/it/responsabili melden.Indem Sie Nebenwirkungen melden, können Sie dazu beitragen, dass mehr Informationen über die Sicherheit dieses Arzneimittels zur Verfügung gestellt werden.
Ablauf und Aufbewahrung
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
Bewahren Sie dieses Arzneimittel für Kinder unzugänglich auf.
Verwenden Sie dieses Arzneimittel nicht nach dem Verfallsdatum, das auf der Packung nach Verfallsdatum angegeben ist. Das Ablaufdatum bezieht sich auf den letzten Tag dieses Monats.
Werfen Sie Arzneimittel nicht in das Abwasser oder den Hausmüll. Fragen Sie Ihren Apotheker, wie Sie Arzneimittel, die Sie nicht mehr verwenden, entsorgen. Dies trägt zum Schutz der Umwelt bei.
Frist "> Weitere Informationen
Was Sandomigran enthält
- Der Wirkstoff ist Pizotifenmalatsäure. Jede überzogene Tablette enthält 0,73 mg Pizotifen-Malatsäure (entsprechend 0,50 mg Pizotifen).
- Die sonstigen Bestandteile sind Magnesiumstearat, Talkum, Povidon, Maisstärke, Lactose-Monohydrat, Titandioxid, hydriertes Erdnussöl, hochdisperses Siliciumdioxid, Macrogol 6000, Saccharose, Stearinsäure, mikrokristalline Cellulose, Cetylalkohol.
Beschreibung des Aussehens von Sandomigran und Inhalt der Packung
Jede Packung Sandomigran 0,5 mg überzogene Tabletten enthält 20 überzogene Tabletten.
Quelle Packungsbeilage: AIFA (Italienische Arzneimittelbehörde). Im Januar 2016 veröffentlichter Inhalt. Die vorliegenden Informationen können nicht aktuell sein.
Um Zugriff auf die aktuellste Version zu erhalten, ist es ratsam, auf die Website der AIFA (Italienische Arzneimittelbehörde) zuzugreifen. Haftungsausschluss und nützliche Informationen.
01.0 BEZEICHNUNG DES ARZNEIMITTELS -
SANDOMIGRAN 0,5 MG ÜBERZOGENE TABLETTEN
02.0 QUALITATIVE UND QUANTITATIVE ZUSAMMENSETZUNG -
1 überzogene Tablette enthält:
Wirkprinzip:
Pizotifen-Malatsäure ................................................................. 0,730 mg
(entspricht 0,50 mg Base).
Hilfsstoffe mit bekannter Wirkung : Lactose-Monohydrat, gehärtetes Erdnussöl, Saccharose.
Vollständige Auflistung der sonstigen Bestandteile siehe Abschnitt 6.1.
03.0 DARREICHUNGSFORM -
Dragees.
04.0 KLINISCHE INFORMATIONEN -
04.1 Anwendungsgebiete -
Prophylaktische Behandlung von wiederkehrenden vaskulären Kopfschmerzen, wie:
- Typische oder atypische Migräne
- Cluster-Kopfschmerz
Die International Classification of Headache Disorders 2nd Edition (ICHD-II) ist eine von Ärzten verwendete Standardklassifikation von Kopfschmerzen und beschreibt die oben genannten Erkrankungen wie folgt: prophylaktische Behandlung rezidivierender Migräne mit oder ohne Aura und Cluster-Kopfschmerz.
Sandomigran ist nicht angezeigt, um die laufende Migräneattacke zu stoppen.
04.2 Dosierung und Art der Anwendung -
Durchschnittsbevölkerung
Beginnen Sie mit 0,5 mg pro Tag; die Dosis kann schrittweise erhöht werden. Die durchschnittliche Erhaltungsdosis beträgt 1,5 mg pro Tag in aufgeteilten Dosen oder als Einzeldosis am Abend. In besonders resistenten Fällen kann der Arzt nach und nach Dosierungen von bis zu 3 - 4,5 mg pro Tag, aufgeteilt auf 3 Dosen, erreichen.
Kinder und Jugendliche (Kinder und Jugendliche ab 2 Jahren An)
Beginnen Sie mit 0,5 mg; die Dosis kann auf 1,5 mg in geteilten Dosen oder 1 mg als Einzeldosis am Abend erhöht werden. Sandomigran sollte älteren Kindern nicht gegeben werden weniger als 2 Jahre (siehe 4.3).
Besondere Bevölkerungsgruppen
Nieren- und Leberinsuffizienz
Bei Patienten mit Nieren- und Leberinsuffizienz ist Vorsicht geboten und eine Dosisanpassung kann erforderlich sein (siehe Abschnitt 5.2 Klinische Pharmakologie / Pharmakokinetik / Besondere Patientengruppen).
04.3 Kontraindikationen -
Überempfindlichkeit gegen den Wirkstoff oder einen der in Abschnitt 6.1 genannten sonstigen Bestandteile. Sandomigran sollte älteren Kindern nicht gegeben werden weniger als 2 Jahre.
In Schwangerschaft und Stillzeit kontraindiziert (siehe Abschnitt 4.6).
04.4 Besondere Warnhinweise und geeignete Vorsichtsmaßnahmen für die Anwendung -
Es wurde über Leberschäden berichtet, die von erhöhten Transaminasen bis hin zu schwerer Hepatitis reichen. Die Behandlung mit Pizotifen sollte abgebrochen werden, wenn während der Behandlung klinische Hinweise auf eine Leberfunktionsstörung vorliegen und bis die Ursache der Leberanomalie geklärt ist. Pizotifen sollte bei Patienten mit bekannter oder vermuteter Leberfunktionsstörung mit Vorsicht angewendet werden, die sich in regelmäßigen Abständen angemessenen Labortests unterziehen sollten.
Pizotifen hat eine leichte anticholinerge Wirkung und daher ist bei der Behandlung von Patienten mit unbehandeltem Engwinkelglaukom oder Harnverhalt (z. B. Prostatahypertrophie) Vorsicht geboten. Angesichts der Möglichkeit von Akkommodationsstörungen wird empfohlen, auf jede Veränderung des Sehvermögens zu achten.
Bei Epilepsiepatienten wurden häufiger Nebenwirkungen wie Krämpfe beobachtet. Pizotifen sollte bei epileptischen Patienten mit Vorsicht angewendet werden.
Pizotifen hat ein porphyrinogenes Potenzial und sollte bei anfälligen Patienten mit Vorsicht angewendet werden und nur, wenn sicherere Alternativen nicht verfügbar sind.
Absetzsymptome wie Depression, Zittern, Übelkeit, Angst, Unwohlsein, Schwindel, Schlafstörungen und Gewichtsverlust wurden nach abruptem Absetzen von Pizotifen berichtet (siehe Abschnitt 4.8 Nebenwirkungen): Daher wird ein schrittweises Absetzen der Behandlung empfohlen.
Wichtige Informationen zu einigen der Hilfsstoffe
Pizotifen enthält Lactose. Patienten mit der seltenen hereditären Galactose-Intoleranz, Lapp-Lactase-Mangel oder Glucose-/Galactose-Malabsorption sollten dieses Arzneimittel nicht einnehmen.
Pizotifen enthält gehärtetes Erdnussöl. Raffiniertes Erdnussöl kann Erdnussproteine enthalten. Die Monographie des Europäischen Arzneibuchs sieht keinen Assay auf Restproteine vor.
Pizotifen enthält Saccharose. Patienten mit der seltenen hereditären Fructoseintoleranz, Glucose-Galactose-Malabsorption oder Saccharase-Isomaltase-Mangel sollten dieses Arzneimittel nicht einnehmen.
04.5 Wechselwirkungen mit anderen Arzneimitteln und sonstige Wechselwirkungen -
Die folgenden Arzneimittel können in Kombination mit Pizotifen Arzneimittelwechselwirkungen aufweisen.
Zu berücksichtigende bekannte Wechselwirkungen
Pizotifen wird weitgehend in der Leber metabolisiert, hauptsächlich durch N-Glucuronidierung. Ein Anstieg der Plasmakonzentration von Pizotifen bei gleichzeitiger Gabe von ausschließlich glukuronidierten Arzneimitteln kann nicht ausgeschlossen werden.
Cisaprid
Die gleichzeitige Anwendung von Pizotifen mit Cisaprid kann zu einer verminderten Wirksamkeit von Cisaprid führen.
Adrenerge Blocker
Pizotifen antagonisiert die blutdrucksenkende Wirkung von adrenergen Blockern.
Wirkstoffe des zentralen Nervensystems
Pizotifen kann die zentrale Wirkung von Sedativa, Hypnotika, Antihistaminika (einschließlich einiger Erkältungspräparate) und Alkohol verstärken.
Die anticholinerge Wirkung von Pizotifen kann durch die gleichzeitige Einnahme von I-MAO verlängert und verstärkt werden.
04.6 Schwangerschaft und Stillzeit -
Schwangerschaft
Zur Anwendung von Pizotifen in der Schwangerschaft liegen nur begrenzte Daten vor, daher ist es ratsam, Sandomigran während der Schwangerschaft nur bei eindeutiger Notwendigkeit zu verschreiben (siehe Abschnitt 4.3).
Fütterungszeit
Obwohl die in der Milch von behandelten Müttern gefundenen Pizotifen-Konzentrationen wahrscheinlich keinen Einfluss auf das Neugeborene haben, wird die Anwendung von Sandomigran während der Stillzeit nicht empfohlen (siehe Abschnitt 4.3).
Fruchtbarkeit
Studien an männlichen und weiblichen Ratten, selbst bei den höchsten bewerteten Dosierungen, 30 mg / kg, zeigten keine Auswirkungen auf Fertilität, Wurfgröße, Überlebensrate, Missbildungen oder Gewichtszunahme der Nachkommen.
04.7 Auswirkungen auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen -
Maschinen
Pizotifen hat einen großen Einfluss auf die Verkehrstüchtigkeit und die Fähigkeit zum Bedienen von Maschinen.
Pizotifen kann Sedierung, Schläfrigkeit und Schwindel verursachen. Daher ist beim Führen von Fahrzeugen oder beim Bedienen von Maschinen Vorsicht geboten.
Patienten, die mit Pizotifen mit Episoden von Sedierung und/oder Schläfrigkeit behandelt werden, sollten sensibilisiert werden, weder Auto zu fahren noch Aktivitäten nachzugehen, bei denen eine eingeschränkte Aufmerksamkeit sich selbst oder andere gefährden kann.
04.8 Nebenwirkungen -
Nebenwirkungen werden nach Häufigkeit nach der folgenden Konvention aufgelistet: Sehr häufig (≥ 1/10); häufig (≥ 1/100,
Die häufigsten Nebenwirkungen sind: Appetitanregung, Gewichtszunahme und Sedierung (einschließlich Schläfrigkeit und Müdigkeit).
Tabelle 1
Unerwünschte Arzneimittelwirkungen aus Spontanberichten nach Markteinführung
Die folgenden zusätzlichen Nebenwirkungen, die auf Spontanberichten nach der Markteinführung beruhen, wurden mit Pizotifen beobachtet. Da diese Reaktionen freiwillig aus einer Population ungewisser Größe gemeldet wurden, ist es nicht immer möglich, ihre Häufigkeit zuverlässig abzuschätzen.
Leber- und Gallenerkrankungen
Erhöhte Leberenzyme, Gelbsucht, Hepatitis.
Muskel-Skelett- und Bindegewebserkrankungen
Muskelkrämpfe.
Entzugserscheinungen
Nach einem abrupten Absetzen von Pizotifen wurden Absetzreaktionen beobachtet, daher wird ein schrittweises Absetzen der Behandlung empfohlen (siehe Abschnitt 4.4). Entzugssymptome können sein: Depression, Zittern, Übelkeit, Angst, Unwohlsein, Schwindel, Schlafstörungen, Gewichtsverlust und Bewusstlosigkeit.
Meldung von vermuteten Nebenwirkungen
Die Meldung von vermuteten Nebenwirkungen, die nach der Zulassung des Arzneimittels auftreten, ist wichtig, da sie eine kontinuierliche Überwachung des Nutzen-Risiko-Verhältnisses des Arzneimittels ermöglicht. Angehörige von Gesundheitsberufen werden gebeten, jeden Verdachtsfall einer Nebenwirkung über das nationale Meldesystem zu melden. "Adresse www. agenziafarmaco.gov.it/it/responsabili.
04.9 Überdosierung -
Symptome: Benommenheit, Übelkeit, Erbrechen, Mundtrockenheit, Tachykardie, Fieber, Hypotonie, Dyspnoe, Zyanose, Schwindel, Verwirrtheit, Ataxie, Sedierung, ZNS-Depression, Erregungszustand (bei Kindern), Atemdepression, Krämpfe (insbesondere bei Kindern), Koma .
Eine Vergiftung durch Antihistaminika kann bei Kindern Halluzinationen, Koordinationsstörungen, feste und erweiterte Pupillen, Gesichtsrötung und Fieber verursachen, mit möglicher Entwicklung in Richtung Koma und Herz-Kreislauf-Kollaps.
Behandlung: Die Gabe von Aktivkohle wird empfohlen; Magenspülung kann nur bei sehr kurzer Einnahmezeit sinnvoll sein, ggf. symptomatische Behandlung einleiten und kardiovaskuläre und respiratorische Symptome überwachen Benzodiazepine können in Erregungszuständen oder bei Krampfanfällen verabreicht werden.
05.0 PHARMAKOLOGISCHE EIGENSCHAFTEN -
05.1 "Pharmakodynamische Eigenschaften -
Pharmakotherapeutische Gruppe: Anti-Migräne / andere Anti-Migräne.
ATC-Code: N02C X01.
Pizotifen zeichnet sich durch eine polyvalente Hemmwirkung biogener Amine wie Serotonin, Histamin und Tryptamin aus. Es besitzt auch eine antibradykininische und beruhigende Wirkung sowie schwache anticholinerge Eigenschaften. Pizotifen ist indiziert zur Migräneprophylaxe, indem es die Anfallshäufigkeit reduziert.
Pizotifen hat auch appetitanregende Eigenschaften.
05.2 "Pharmakokinetische Eigenschaften -
Absorption
Nach oraler Gabe wird das Arzneimittel schnell und fast vollständig aus dem Magen-Darm-Trakt resorbiert. Die mittlere absolute Bioverfügbarkeit nach oraler Gabe beträgt ca. 80 % Nach einmaliger oraler Gabe von 2 mg Pizotifen betrug die zusammen gemessene mittlere maximale Plasmakonzentration (Cmax) von Pizotifen und seinem Metaboliten ca. 5 ng/ml (Tmax 5,5 Std.). Verabreichung von 1 mg dreimal täglich über sechs Tage, die mittlere maximale Steady-State-Plasmakonzentration wurde 4 Stunden nach der Verabreichung beobachtet (Cmax, ss: 14 ng/ml) und die mittlere Plasma-Talkonzentration betrug ungefähr 11 ng/ml (Cmin, ss).
Verteilung
Pizotifen wird mit einem mittleren Verteilungsvolumen von 833 l für die Muttersubstanz bzw. 70 l für ihren N-Glucuronid-Metaboliten weit und schnell im ganzen Körper verteilt. Ungefähr 91 % des Arzneimittels sind an Plasmaproteine gebunden. Verteilungs- und Eliminationskinetiken wurden im Allgemeinen als biexponentielle Zerfallsfunktion mit einem Zwei-Kompartiment-Modell beschrieben.
Stoffwechsel
Pizotifen wird hauptsächlich in der Leber durch Glucuronidierung weitgehend metabolisiert. Der Hauptmetabolit ist konjugiertes N-Glucuronid, das mindestens 50 % der Plasmaexposition ausmacht.
Beseitigung
Etwa ein Drittel der oral verabreichten Dosis wird über die Gallenwege ausgeschieden. Ein erheblicher Anteil des Arzneimittels, der etwa 18 % der verabreichten Dosis entspricht, befindet sich in den Fäzes. Der verbleibende Anteil der verabreichten Dosis (ca. 55 %) wird hauptsächlich als Metaboliten mit dem Urin ausgeschieden. Weniger als 1 % der verabreichten Dosis von Pizotifen wird unverändert über die Nieren ausgeschieden Pizotifen und sein Hauptmetabolit, das konjugierte N-Glucuronid, werden mit einer Halbwertszeit von etwa 23 Stunden eliminiert.
Besondere Bevölkerungsgruppen
Nierenversagen
Bei Patienten mit Niereninsuffizienz wurden keine spezifischen pharmakokinetischen Studien durchgeführt. Da Pizotifen hauptsächlich in Form von Metaboliten mit dem Urin ausgeschieden wird, kann die Möglichkeit einer Akkumulation inaktiver Metaboliten infolge der Akkumulation des Mutterarzneimittels nicht ausgeschlossen werden.
Bei Patienten mit Niereninsuffizienz ist Vorsicht geboten und eine Dosisanpassung kann erforderlich sein.
Leberinsuffizienz
Obwohl bei Patienten mit Leberinsuffizienz keine spezifischen pharmakokinetischen Studien durchgeführt wurden, wird Pizotifen weitgehend in der Leber metabolisiert und hauptsächlich als Glucuronid mit dem Urin ausgeschieden. Vorsicht ist bei Patienten mit Leberinsuffizienz geboten, bei denen eine Dosisanpassung erforderlich sein kann.
05.3 Präklinische Daten zur Sicherheit -
Toxizität bei wiederholter Gabe
Toxizitätsstudien mit wiederholter Gabe von bis zu 2 Jahren Dauer wurden an Ratten und Hunden durchgeführt. Aus histopathologischen Befunden identifizierte Zielorgane waren Leber, Niere und manchmal Schilddrüse bei Ratten und Leber, Schilddrüse und Milz bei Hunden. Der No-Observed-Effect-Level (NOEL) betrug sowohl bei Ratten als auch bei Hunden 3 mg/kg, was dem 30-fachen der maximal empfohlenen Tagesdosis beim Menschen entspricht.
Reproduktionstoxizität
Pytoziphenhydrogenmalat wurde in mehreren Reproduktions- und Entwicklungstoxizitätsstudien auf seine Auswirkungen auf die Fertilität und auf sein embryotoxisches, fetotoxisches, teratogenes und entwicklungstoxisches Potenzial untersucht. Bei Mäusen, Ratten oder Kaninchen wurden bis zu den höchsten getesteten Dosen von 30 mg/kg keine spezifischen Reproduktions- oder Entwicklungseffekte beobachtet. Diese Dosierung ist 300-mal höher als die maximal empfohlene Tagesdosis von 0,09 mg / kg für Erwachsene.
Mutagenität
Mutagenitätstests durchgeführt in vitro Und in vivo zeigten kein mutagenes Potenzial von erkranktem Pizotifen-Wasserstoff.
Karzinogenität
2-Jahres-Toxizitätsstudien an Ratten zeigten keine größeren Läsionen oder Massen, die auf die Verabreichung von Pizotifenhydrogenmalat in Dosen von bis zu 27 mg/kg zurückzuführen waren, einer Dosis, die 300 Mal höher war als die maximal empfohlene Tagesdosis für den Menschen (basierend auf mg/kg). .
06.0 PHARMAZEUTISCHE INFORMATIONEN -
06.1 Hilfsstoffe -
Magnesiumstearat; Talk; Povidon; Maisstärke; Lactosemonohydrat; Titandioxid; gehärtetes Erdnussöl; wasserfreies kolloidales Siliciumdioxid; Macrogol 6000; Saccharose; Stearinsäure; mikrokristalline Cellulose; Cetylalkohol.
06.2 Inkompatibilität "-
Keiner.
06.3 Gültigkeitsdauer "-
5 Jahre.
06.4 Besondere Vorsichtsmaßnahmen für die Aufbewahrung -
Für dieses Arzneimittel sind keine besonderen Lagerungsbedingungen erforderlich.
06.5 Art der unmittelbaren Verpackung und Inhalt des Packstücks -
Blisterpackung mit 20 überzogenen Tabletten.
06.6 Gebrauchs- und Handhabungshinweise -
Keine besonderen Anweisungen.
07.0 INHABER DER "MARKETING GENEHMIGUNG" -
PHOENIX LABS - Suite 12, Bunkilla Place, Bracetown Buusiness Park, Clonee Co Meath, Irland
08.0 NUMMER DER VERMARKTUNGSBERECHTIGUNG -
A.I.C. n. 022437014
09.0 DATUM DER ERSTEN GENEHMIGUNG ODER ERNEUERUNG DER GENEHMIGUNG -
Erstautorisierung: 29.12.1971
Erneuerung: 01.06.2010