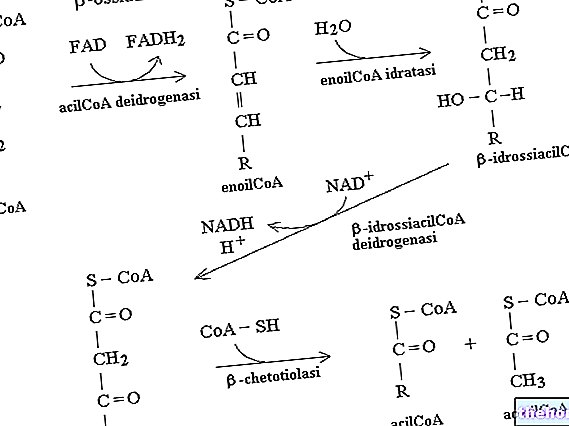
Glykogen ist ein Makromolekül (Molekulargewicht ca. 400 Millionen Dalton) der α-Glucose, in dem hauptsächlich α-1,4-glykosidische Bindungen und Verzweigungen im Verhältnis 1:10 aufgrund von α-1,6-glykosidischen Bindungen vorliegen.
Glykogen stellt Reservematerial dar und wird kontinuierlich abgebaut und rekonstituiert; in der gesamten Zellmasse des Körpers befinden sich etwa 100 g Glykogen: Das meiste davon befindet sich in der Leber, wo es mobil ist und kann daher als Reserve für andere Organe verwendet werden (Glykogen in den Muskeln ist nicht mobil).
Die Enzyme, die den Abbau und die Synthese von Glykogen katalysieren, befinden sich alle im Zytoplasma, daher wird ein Regulationssystem benötigt, das einen Weg inaktiv macht, wenn der andere aktiv ist: Wenn Glukose verfügbar ist, wird diese in Glykogen umgewandelt (Anabolismus). eine Reserve, umgekehrt, wenn c "für Glukose benötigt wird, dann wird das Glykogen abgebaut (Katabolismus).

Das Enzym, das hauptsächlich am Abbau von Glykogen beteiligt ist, ist das Glykogenphosphorylase; Dieses Enzym ist in der Lage, eine glykosidische α-1,4-Bindung unter Verwendung eines anorganischen Orthophosphats als Lysemittel zu spalten: die Spaltung erfolgt auf phosphorolytischem Weg und es wird Glucose-1-phosphat erhalten.
Bei fünf oder sechs Einheiten von einem Verzweigungspunkt ist das Glykogen-Phosphorylase-Enzym nicht mehr handlungsfähig, daher löst es sich vom Glykogen und wird durch ein deramifizierendes Enzym ersetzt, das a Transferase: im katalytischen Zentrum dieses Enzyms ist c "ein" Histidin, das die Übertragung von drei Saccharideinheiten auf die nächste glykosidische Kette ermöglicht (Histidin greift den ersten Kohlenstoff eines Glucosemoleküls an). Das gerade erwähnte Enzym ist das Glykosyltransferase; Am Ende der Wirkung dieses Enzyms verbleibt nur noch eine Glucoseeinheit an der Seitenkette, wobei das erste Kohlenstoffatom an das sechste Kohlenstoffatom einer Glucose in der Hauptkette gebunden ist.Die letzte Glucoseeinheit in der Seitenkette wird durch die Wirkung von . freigesetzt "Enzym α-1,6-Glycosidase (dieses Enzym bildet den zweiten Teil des deramifizierenden Enzyms); da die Verzweigungen im Glykogen in einem Verhältnis von 1:10 stehen, erhalten wir aus dem vollständigen Abbau des Makromoleküls etwa 90% Glucose-1-Phosphat und etwa 10% von Glucose.
Die Wirkung der genannten Enzyme ermöglicht die Abspaltung einer Seitenkette aus dem Glykogenmolekül, deren Aktivität bis zum vollständigen Abbau der Kette wiederholt werden kann.
Betrachten wir einen Hepatozyten; Glukose (über die Nahrung aufgenommen) wird beim Eintritt in die Zelle in Glukose-6-Phosphat umgewandelt und somit aktiviert. Glucose-6-phosphat, durch die Wirkung von Phosphoglucomutase, wird in Glucose-1-phosphat umgewandelt: Letzteres ist eine nicht unmittelbare Vorstufe der Biosynthese; bei der Biosynthese wird eine aktivierte Form von Zuckern verwendet, die durch Zucker dargestellt wird, der an ein Diphosphat gebunden ist: normalerweise Uridyldiphosphat (UDP). dann in UDP-Glucose umgewandelt, dieser Metabolit unter der Wirkung von Glykogensynthase die in der Lage ist, UDP-Glucose an ein nicht-reduzierendes Ende des wachsenden Glykogens zu binden: Man erhält verlängertes Glykogen einer Glucosideinheit und UDP UDP wird durch das nukleosidierte Diphosphokinase-Enzym in UTP umgewandelt, das in den Kreislauf zurückkehrt.
Der Abbau von Glykogen erfolgt durch die Wirkung von Glykogenphosphorylase die ein Glukosemolekül freisetzt und in Glukose-1-phosphat umwandelt. Anschließend wandelt Phosphoglucomutase Glucose-1-phosphat in Glucose-6-phosphat um.
Glykogen wird vor allem in Leber und Muskulatur synthetisiert: Im Organismus sind 1-1,2 Hektogramm Glykogen über die Muskelmasse verteilt.
Das Glykogen einer Myozyte stellt nur für diese Zelle eine Energiereserve dar, während das in der Leber enthaltene Glykogen auch eine Reserve für andere Gewebe darstellt, dh als Glukose an andere Zellen gesendet werden kann.
Das in der Muskulatur beim Abbau von Glykogen gewonnene Glukose-6-phosphat wird dann bei Energiebedarf der Glykolyse zugeführt; in der Leber wird Glucose-6-phosphat durch die Wirkung von in Glucose umgewandelt Glucose-6-Phosphat-Phosphatase (charakteristisches Enzym der Hepatozyten) und gelangt in die Blutbahn.
Glykogen-Synthase und Glykogen-Phosphorylase wirken beide auf die nicht-reduzierenden Einheiten des Glykogens, daher muss ein hormonelles Signal vorliegen, das die Aktivierung des einen Signalwegs und die Blockierung des anderen (oder umgekehrt) befehligt.
Im Labor konnte die Glykogenkette durch Ausnutzung der Glykogenphosphorylase und Verwendung von Glucose-1-Phosphat in sehr hoher Konzentration verlängert werden.
In Zellen katalysiert die Glykogen-Phosphorylase nur die Abbaureaktion, weil die Konzentrationen der Metaboliten das Gleichgewicht der folgenden Reaktion nach rechts (dh in Richtung des Abbaus von Glykogen) verschieben:

Sehen wir uns den Wirkmechanismus der Glykogen-Phosphorylase an: Der Acetal-Sauerstoff (der als Brücke zwischen den Glukose-Einheiten fungiert) bindet an den Wasserstoff des Phosphoryls: Es entsteht ein Reaktionszwischenprodukt durch ein Carbokation (auf der Glukose, die alle " Extremitäten), an die Phosphoryl (Pi) sehr schnell bindet.
Glykogen-Phosphorylase benötigt einen Cofaktor, der Pyridoxalphosphat ist (dieses Molekül ist auch ein Cofaktor für Transaminasen): Sie hat ein teilweise protoniertes Phosphoryl (Pyridoxalphosphat ist von einer hydrophoben Umgebung umgeben, die das Vorhandensein von daran gebundenen Protonen rechtfertigt). Das Phosphoryl (Pi) ist in der Lage, ein Proton auf das Glykogen zu übertragen, da dieses Phosphoryl dann das Proton aus dem teilweise protonierten Phosphoryl des Pyridoxalphosphats zurückerhält. Die Wahrscheinlichkeit, dass das Phosphoryl bei physiologischem pH sein Proton verliert und vollständig deprotoniert bleibt, ist sehr gering.
Sehen wir uns nun an, wie Phosphoglucomutase funktioniert.Dieses Enzym präsentiert im katalytischen Zentrum einen Rest von phosphoryliertem Serin; Serin liefert Phosphoryl zu Glucose-1-phosphat (in Position sechs): Glucose-1,6-bisphosphat wird für kurze Zeit gebildet, dann wird Serin rephosphoryliert, wobei das Phosphoryl in Position eins zurückgenommen wird. Phosphogluco-Mutase kann in beide Richtungen wirken, dh Glucose-1-phosphat in Glucose-6-phosphat umwandeln oder umgekehrt; Wird Glukose-6-Phosphat gebildet, kann es direkt zur Glykolyse in die Muskeln geleitet oder in der Leber in Glukose umgewandelt werden.
Das Enzym Uridyl-Phosphogluco-Transferase (oder UDP-Glucose-Pyrophosphorylase) katalysiert die Glucose-1-Phosphat-Transferreaktion auf UTP durch Anlagerung an Phosphoryl a.
Das gerade beschriebene Enzym ist eine Pyrophosphorylase: Dieser Name ist darauf zurückzuführen, dass die entgegengesetzte Reaktion zu der eben beschriebenen eine Pyrophosphorylierung ist.
UDP-Glucose, wie beschrieben gewonnen, ist in der Lage, die Glykogenkette um eine Monosaccharid-Einheit zu verlängern.
Es ist möglich, die Reaktion zur Bildung von UDP-Glucose zu entwickeln, indem man ein Pyrophosphat-Produkt eliminiert; das Enzym Pyrophosphatase wandelt Pyrophosphat in zwei Moleküle Orthophosphat um (Hydrolyse eines Anhydrids) und hält dabei die Pyrophosphatkonzentration so niedrig, dass der Prozess der Bildung von UDP-Glukose thermodynamisch begünstigt wird.
Wie bereits erwähnt, ist UDP-Glucose dank der Wirkung der Glykogensynthase in der Lage, die Glykogenkette zu verlängern.
Die Auswirkungen (im Verhältnis 1:10) sind darauf zurückzuführen, dass bei einer Glykogenkette, die aus 20-25 Einheiten besteht, ein Verzweigungsenzym (mit einem "Histidin an seiner katalytischen Stelle") eingreift, das in der Lage ist, eine Reihe von 7 -8 glykosidische Einheiten weiter stromabwärts von 5-6 Einheiten: dadurch wird eine neue Verzweigung erzeugt.
Aus nervösen Gründen oder wenn durch körperliche Anstrengung Energie benötigt wird, wird Adrenalin aus den Nebennieren ausgeschüttet.
Die Zielzellen von Adrenalin (und Noradrenalin) sind die der Leber, der Muskulatur und des Fettgewebes (in letzterem findet der Abbau von Triglyceriden und die Zirkulation von Fettsäuren statt: folglich wird in den Mitochondrien Glukose produziert 6-Phosphat, um zur Glykolyse geschickt, während in Adipozyten Glucose-6-Phosphat durch die Wirkung des Enzyms Glucose-6-Phosphat-Phosphatase in Glucose umgewandelt und in das Gewebe exportiert wird).
Sehen wir uns nun die Wirkungsmodalitäten von Adrenalin an. Adrenalin bindet an einen Rezeptor auf der Zellmembran (von Myozyten und Hepatozyten) und bestimmt die Übertragung des Signals von außen nach innen.Die Proteinkinase wird aktiviert, die gleichzeitig auf die Systeme einwirkt, die die Synthese und den Abbau von Glykogen regulieren:
Glykogensynthase existiert in zwei Formen: einer dephosphorylierten (aktiven) Form und einer phosphorylierten (inaktiven) Form; Proteinkinase phosphoryliert die Glykogensynthase und blockiert ihre Wirkung.
Glykogenphosphorylase kann in zwei Formen vorliegen: einer aktiven Form, in der ein phosphoryliertes Serin vorhanden ist, und einer inaktiven Form, in der Serin dephosphoryliert ist. Glykogenphosphorylase kann durch das Enzym aktiviert werden Glykogen-Phosphorylase-Kinase. Glykogen-Phosphorylase-Kinase ist aktiv, wenn sie phosphoryliert ist, und inaktiv, wenn sie dephosphoryliert ist; die Proteinkinase hat als Substrat die Glykogen-Phosphorylase-Kinase, dh sie kann diese phosphorylieren (und damit aktivieren), was wiederum die Glykogen-Phosphorylase aktiviert.
Ist das Adrenalin-Signal vorbei, muss auch die Wirkung auf die Zelle enden: Phosphatase-Enzyme greifen dann auf die Proteinspezies ein.