Was ist Benlysta-Belimumab?
Benlysta ist ein Pulver zur Herstellung einer Infusionslösung (Tropfinfusion in eine Vene), die den Wirkstoff Belimumab enthält.
Wofür wird Benlysta verwendet?
Benlysta ist als Zusatztherapie bei Erwachsenen mit Autoantikörper-positivem systemischem Lupus erythematodes (SLE) mit hoher Krankheitsaktivität trotz Standardtherapie angezeigt.
Das Arzneimittel ist nur auf ärztliche Verschreibung erhältlich.
Wie wird Benlysta - Belimumab angewendet?
Die Behandlung mit Benlysta sollte von einem in der Diagnose und Behandlung von SLE erfahrenen Arzt eingeleitet und überwacht werden.
Benlysta wird als intravenöse Infusion über „eine“ Stunde verabreicht. Die empfohlene Dosis beträgt 10 mg pro Kilogramm Körpergewicht. Die ersten drei Dosen werden in zweiwöchigen Abständen verabreicht. Danach wird Benlysta in vierwöchigen Abständen eingenommen.
Der Arzt muss möglicherweise erwägen, die Behandlung zu unterbrechen oder abzubrechen, wenn der Patient Infusionsreaktionen (einschließlich Erythem, Juckreiz und Atembeschwerden) oder Überempfindlichkeitsreaktionen (allergische) entwickelt. Benlysta sollte daher nur in einer Umgebung verabreicht werden, in der solche Reaktionen sofort behandelt werden können .
Wie wirkt Benlysta - Belimumab?
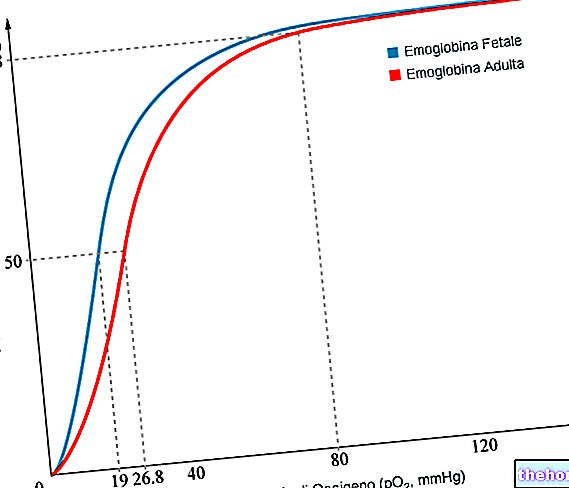
SLE ist eine Krankheit, bei der das Immunsystem (die natürlichen Abwehrkräfte des Körpers) die Zellen und Gewebe des Patienten angreift und Entzündungen und Schäden an verschiedenen Organen verursacht.Sie kann fast jedes Organ betreffen und soll eine Art von weißen Blutkörperchen namens B-Lymphozyten betreffen. B-Lymphozyten produzieren im Allgemeinen Antikörper (Proteine), die bei der Bekämpfung von Infektionen helfen.Bei SLE greifen einige dieser Antikörper die Zellen und Organe des Körpers an (Autoantikörper).
Der Wirkstoff in Benlysta, Belimumab, ist ein monoklonaler Antikörper. Ein monoklonaler Antikörper ist ein Antikörper, der entwickelt wurde, um eine im Körper vorhandene spezifische Struktur (das Antigen) zu erkennen und daran zu binden. Belimumab wurde entwickelt, um ein Protein namens BLyS zu binden und zu blockieren, das B-Lymphozyten hilft, länger zu leben. Durch die Blockierung der Wirkung von BLyS verkürzt Belimumab die Lebensdauer von B-Lymphozyten und reduziert dadurch die bei SLE beobachteten Entzündungen und Organschäden.
Wie wurde Benlysta - Belimumab untersucht?
Die Wirkung von Benlysta wurde zunächst in experimentellen Modellen getestet, bevor sie am Menschen untersucht wurde.
Benlysta (verabreicht in Dosen von 1 und 10 mg/kg Körpergewicht) wurde in zwei Hauptstudien mit 1.693 erwachsenen Patienten mit aktivem SLE mit Placebo (einer Scheinbehandlung) verglichen. Die Patienten erhielten während der gesamten Studien weiterhin eine Standard-SLE-Therapie. In beiden Studien war der Hauptindikator für die Wirksamkeit die Anzahl der Patienten, deren Krankheitsaktivität nach 12 Monaten auf ein bestimmtes Niveau abnahm.
Welchen Nutzen hat Benlysta - Belimumab in den Studien gezeigt?
Benlysta erwies sich bei der Verringerung der Krankheitsaktivität bei der Verringerung der Krankheitsaktivität als wirksamer als Placebo, wenn es als Zusatztherapie bei SLE angewendet wurde In der zweiten Studie war die Benlysta-Dosis von 10 mg/kg bei 58 % der Patienten wirksam, verglichen mit 44 % der mit Placebo behandelten Patienten. In beiden Studien war die Benlysta-Dosis von 10 mg/kg wirksamer als die 1 mg / kg Dosis.
Welches Risiko ist mit Benlysta - Belimumab verbunden?
Sehr häufige Nebenwirkungen von Benlysta (beobachtet bei mehr als 1 von 10 Patienten) sind Durchfall und Übelkeit. Die vollständige Liste der von Benlysta berichteten Nebenwirkungen finden Sie in der Packungsbeilage.
Benlysta darf nicht bei Patienten angewendet werden, die möglicherweise überempfindlich (allergisch) gegen Belimumab oder einen der anderen Stoffe sind.
Warum wurde Benlysta - Belimumab zugelassen?
Der CHMP war der Ansicht, dass Benlysta als Zusatztherapie bei SLE-Patienten die Krankheitsaktivität ohne ernsthaftes Risiko für den Patienten reduziert.Das Arzneimittel kann Überempfindlichkeits- und Infusionsreaktionen sowie Infektionen verursachen, wird aber im Allgemeinen gut vertragen stellte außerdem fest, dass es keine wirksamen alternativen Therapien für Patienten gibt, die bereits eine Standardbehandlung erhalten haben.Der Ausschuss entschied, dass der Nutzen von Benlysta gegenüber seinen Risiken überwiegt, und empfahl die Genehmigung für das Inverkehrbringen.
Weitere Informationen zu Benlysta - belimumab
Am 13. Juli 2011 hat die Europäische Kommission eine „Marketing Authorization“ für Benlysta ausgestellt, die in der gesamten Europäischen Union gültig ist.
Weitere Informationen zur Benlysta-Therapie finden Sie in der Packungsbeilage (im EPAR enthalten) oder wenden Sie sich an Ihren Arzt oder Apotheker.
Letzte Aktualisierung dieser Zusammenfassung: 07-2011.
Die auf dieser Seite veröffentlichten Informationen zu Benlysta - Belimumab können veraltet oder unvollständig sein. Informationen zur korrekten Verwendung dieser Informationen finden Sie auf der Seite Haftungsausschluss und nützliche Informationen.













-cos-cause-sintomi-e-cura.jpg)